题目内容
9.向含有c(FeCl3)=0.2mol•L-1、c(FeCl2)=0.1mol•L-1的混合溶液中滴加稀NaOH溶液,可得到一种黑色分散系,其中分散质粒子是直径约为9.3nm的金属氧化物,下列有关说法中正确的是( )| A. | 该分散系的分散质为Fe2O3 | |
| B. | 可用过滤的方法将黑色金属氧化物与Na+分离开 | |
| C. | 在电场作用下,阴极附近分散系黑色变深,则说明该分散系带正电荷 | |
| D. | 加入NaOH时发生的反应可能为:Fe2++2Fe3++8OH-═Fe3O4+4H2O |
分析 A.三氧化二铁为红棕色;
B.分散质粒子是直径约为9.3nm,介于1nm-100nm,属于胶体;
C.胶体不带电;
D.依据题意向含有c(FeCl3)=0.2mol•L-1、c(FeCl2)=0.1mol•L-1的混合溶液中滴加稀NaOH溶液,可得到一种黑色分散系,可知该黑色固体为四氧化三铁,据此写出方程式.
解答 解:A.三氧化二铁为红棕色,由题意知得到一种黑色分散系,故A错误;
B.胶体、溶液都可以透过滤纸,不能用过滤方法分离,故B错误;
C.在电场作用下,阴极附近分散系黑色变深,则说明该分散系容易吸附带正电的阳离子而形成带电的胶体微粒,故C错误;
D.氯化亚铁、氯化铁与氢氧化钠反应生成四氧化三铁和水、氯化钠,离子方程式:Fe2++2Fe3++8OH-═Fe3O4+4H2O,故D正确;
故选:D.
点评 本题考查了铁的化合物的性质、胶体的性质,准确把握题意,明确胶体的性质是解题关键,题目难度不大.

练习册系列答案
相关题目
4.下列关于溶液中离子的说法正确的是( )
| A. | 0.1 mol•L-1的Na2CO3溶液中离子浓度关系:c (Na+)=2c (CO32-)+c (HCO3-)+c (H2CO3) | |
| B. | 0.1 mol•L-1的NH4Cl和0.1 mol•L-1的NH3•H2O等体积混合后溶液中的离子浓度关系:c (Cl-)>c (NH4+)>c (H+)>c (OH-) | |
| C. | 常温下,醋酸钠溶液中滴加少量醋酸使溶液的pH=7,则混合溶液中,离子浓度关系:c (Na+)>c (CH3COO-) | |
| D. | 0.1 mol•L-1的NaHS溶液中离子浓度关系:c (OH-)=c (H+)-c (S2-)+c (H2S) |
14.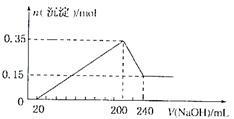 将一定质量Mg和Al的混合物投人500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加人Na0H溶液.生成沉淀的物质的量与加人Na0H溶液体积的关系如图所示.则下列说法正确的是( )
将一定质量Mg和Al的混合物投人500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加人Na0H溶液.生成沉淀的物质的量与加人Na0H溶液体积的关系如图所示.则下列说法正确的是( )
 将一定质量Mg和Al的混合物投人500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加人Na0H溶液.生成沉淀的物质的量与加人Na0H溶液体积的关系如图所示.则下列说法正确的是( )
将一定质量Mg和Al的混合物投人500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加人Na0H溶液.生成沉淀的物质的量与加人Na0H溶液体积的关系如图所示.则下列说法正确的是( )| A. | Mg和A1的总质量为8g | |
| B. | 硫酸的物质的量浓度为5mol•L-1 | |
| C. | 生成的H2在标准状况下的体积为11.2L | |
| D. | Na0H溶液的物质的量浓度为5mo1•L-1 |
19.广口瓶在基础化学实验中应用广泛,下列由广口瓶组装的装置及其操作与应用正确的是( )
| 选项 | 装置 | 操作与应用 |
| A | 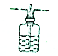 | 在广口瓶中盛放蒸馏水,用于吸收在水中溶解度较小的气体 |
| B | 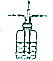 | 在广口瓶中盛放浓硫酸,左右导管中分别通入H2和N2,并按比例混合这两种气体 |
| C |  | 在广口瓶中盛放蒸馏水,用于测定易溶于水的气体的体积 |
| D | 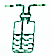 | 在广口瓶中盛放蒸馏水,用于吸收易溶于水的气体 |
| A. | A | B. | B | C. | C | D. | D |