题目内容
【题目】铅蓄电池是典型的可充型电池,它的正负极是情性材料,放电时的电池总反应式为:Pb+PbO2+4H++2SO42-![]() 2PbSO4+2H2O。请回答下列问题,放电时正极的电极反应式是________________________;正极区pH值将____(填“变大”、“变小”或“不变”);电解液中H2SO4的浓度将_____(填“变大”、“变小”或“不变”);当外电路通过1mol电子时,理论上负极板的质量___(填“增加”或“减小”)________g。
2PbSO4+2H2O。请回答下列问题,放电时正极的电极反应式是________________________;正极区pH值将____(填“变大”、“变小”或“不变”);电解液中H2SO4的浓度将_____(填“变大”、“变小”或“不变”);当外电路通过1mol电子时,理论上负极板的质量___(填“增加”或“减小”)________g。
【答案】 PbO2 +2e-+ 4H+ +2SO42-= PbSO4 + 2H2O 变大 变小 增加 48
【解析】分析:根据原电池的工作原理,即负极发生失去电子的氧化反应,正极发生得到电子的还原反应,结合总反应式解答。
详解:根据总反应式可知放电时二氧化铅得到电子生成硫酸铅,则放电时正极的电极反应式是PbO2+2e-+4H++2SO42-=PbSO4+2H2O;由于正极消耗硫酸,氢离子浓度减小,则正极区pH值将变大;放电时消耗硫酸,则电解液中H2SO4的浓度将变小;负极铅失去电子,生成硫酸铅:Pb-2e-+SO42-=PbSO4,因此当外电路通过1mol电子时,理论上负极板的质量增加0.5mol×96g/mol=48g。

【题目】某同学学习了化学反应速率后,联想到曾用H2O2制备氧气,于是设计了下面的实验方案并进行实验探究。
实验编号 | 反 应 物 | 催 化 剂 |
甲 | 试管中加入3 mL 2﹪ H2O2溶液和3滴蒸馏水 | 无 |
乙 | 试管中加入3 mL 5﹪ H2O2溶液和3滴蒸馏水 | 无 |
丙 | 试管中加入3 mL 5﹪ H2O2溶液和3滴蒸馏水 | 1 mL 0.1 mol/L FeCl3溶液 |
丁 | 试管中加入3 mL 5﹪ H2O2溶液和3滴稀盐酸溶液 | 1 mL 0.1 mol/L FeCl3溶液 |
戊 | 试管中加入3 mL 5﹪ H2O2溶液和3滴NaOH溶液 | 1 mL 0.1 mol/L FeCl3溶液 |
【查阅资料】过氧化氢(H2O2),其水溶液俗称双氧水,常温下是一种无色液体,性质比较稳定。在加热的条件下,它能分解生成氧气。研究表明,将新制的5﹪的H2O2溶液加热到65℃时就有氧气放出,加热到80℃时就有较多氧气产生。
(1)上述实验发生反应的化学方程式为 。
(2)实验甲和实验乙的实验目的是 ;
实验丙、实验丁和实验戊的实验目的是 。
(3)请根据该同学查阅的资料分析H2O2的性质,解释实验甲和实验乙能否达到实验目的? 。
(4)实验过程中该同学对实验丙、丁、戊中产生的气体进行收集,并在2分钟内6个时间点对注射器内气体进行读数,记录数据如下表。
时间/s | 20 | 40 | 60 | 80 | 100 | 120 | |
气体体积/mL | 实验丙 | 9.5 | 19.5 | 29.0 | 36.5 | 46.0 | 54.5 |
实验丁 | 8.0 | 16.0 | 23.5 | 31.5 | 39.0 | 46.5 | |
实验戊 | 15.5 | 30.0 | 44.5 | 58.5 | 71.5 | 83.0 | |
①对实验戊,0~20 s的反应速率v1= mL/s,100~120 s的反应速率v2= mL/s。
不考虑实验测量误差,二者速率存在差异的主要原因是 。
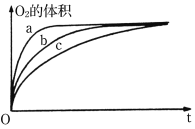
②如右图是根据实验收集到最大体积的气体时所用时间绘制的图像。曲线c表示的是实验 (填“丙”、“丁”或“戊”)。