题目内容
11.已知有如下反应可以发生:HCl+NaOH=NaCl+H2O,浓硫酸可吸水,CuSO4(白)+5H2O═CuSO4•5H2O(蓝).如图所示,将锌粒放入盛有稀盐酸容器中,反应发生一段时间后,给装置D中的药品加热,稍后可见E中白色粉末变蓝.请回答:
(1)E中白色粉末变蓝说明D中反应产物有H2O生成,装置A中发生反应的化学方程式为Zn+2HCl=ZnCl2+H2↑,装置D中发生反应的化学方程式为H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
(2)装置B的作用是吸收稀盐酸挥发出的氯化氢气体,装置C的作用是干燥H2.
(3)A装置中反应发生一段时间后,再给装置D中药品加热,其目的是排尽试管内空气,防止加热时,H2与空气混合发生爆炸.
分析 (1)白色的硫酸铜遇到水变蓝,据此可检验是否有水生成;装置A中锌与稀盐酸反应生成硫酸锌和氢气,据此写出反应的化学方程式;装置D中氧化铜与氢气发生反应生成铜和水.
(2)根据氯化氢具有挥发性可知获得的氢气中混有氯化氢,需要用氢氧化钠溶液除去;氢气与氧化铜的反应需要加热,则氢气必须是干燥的;
(3)氢气不纯时会发生爆炸,需要先用制取的氢气赶走装置中空气.
解答 解:(1)白色的硫酸铜遇到水变蓝,所以E中白色粉末变蓝说明D中反应产物有H2O生成;装置A中锌与稀盐酸反应生成氢气,发生反应的化学方程式为:Zn+2HCl=ZnCl2+H2↑;装置D中氢气与氧化铜加热反应生成铜和水,反应的化学方程式为:H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,
故答案为:H2O;Zn+2HCl=ZnCl2+H2↑;H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;
(2)氯化氢具有挥发性,需要用氢氧化钠溶液除去,则装置B的作用是吸收稀盐酸挥发出的氯化氢气体;制取的氢气中混有水,由于氢气与氧化铜的反应需要加热,所以需要用浓硫酸干燥氢气,
故答案为:吸收稀盐酸挥发出的氯化氢气体;干燥H2;
(3)由于氢气不纯时会发生爆炸,则A装置中反应发生一段时间后,用生成的排尽试管内空气,再给装置D中药品加热,防止加热时,H2与空气混合发生爆炸,
故答案为:排尽试管内空气,防止加热时,H2与空气混合发生爆炸.
点评 本题考查了化学实验装置的综合应用,题目难度中等,明确实验目的、实验原理为解答关键,注意掌握常见装置的构造及使用方法,试题培养了学生的化学实验能力.

练习册系列答案
相关题目
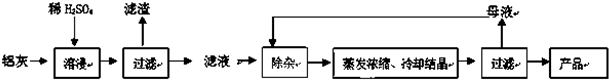
2.用含有A12O3、SiO2和少量FeO•xFe2O3的铝灰制备Al2(SO4)3•18H2O.工艺流程如下:
已知:①一定条件下,MnO4 -可与Mn2+反应生成MnO2
②部分金属阳离子生成氢氧化物沉淀的pH如下表:
③常温下,Fe(OH)3:Ksp=1.1×10-36,Fe(OH)2:Ksp=1.64×10-14,Al(OH)3:Ksp=1.3×10-33
(1)H2SO4溶解A12O3的离子方程式是Al2O3+6H+=2Al3++3H2O
(2)检验滤液中存在Fe3+的方法是取少量滤液于试管,滴加KSCN溶液,溶液变为红色,则滤液中有Fe3+(注明试剂、现象).
(3)“除杂”环节有如下几个步骤:
(Ⅰ)向滤液中加入过量KMnO4溶液,调节溶液的pH为3.7;
(Ⅱ)加热,产生大量红褐色沉淀,静置,上层溶液呈紫红色;
(Ⅲ)加入MnSO4至紫红色消失,过滤.
①步骤Ⅰ的目的:将Fe2+氧化为Fe3+;调节溶液的pH为3.7的目的是调节pH值使铁元素沉淀完全,此时溶液中c(Fe3+)为1.1×10-5.1mol•L-1
②向Ⅱ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是生成有黄绿色气体,写出其反应方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
③Ⅲ中加入MnSO4的目的是除去过量的MnO4-.
(4)从多次循环使用后母液中可回收的主要物质是K2SO4(填化学式)

已知:①一定条件下,MnO4 -可与Mn2+反应生成MnO2
②部分金属阳离子生成氢氧化物沉淀的pH如下表:
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.8 | 6.3 | 2.7 |
| 完全沉淀时 | 5.2 | 9.7 | 3.7 |
(1)H2SO4溶解A12O3的离子方程式是Al2O3+6H+=2Al3++3H2O
(2)检验滤液中存在Fe3+的方法是取少量滤液于试管,滴加KSCN溶液,溶液变为红色,则滤液中有Fe3+(注明试剂、现象).
(3)“除杂”环节有如下几个步骤:
(Ⅰ)向滤液中加入过量KMnO4溶液,调节溶液的pH为3.7;
(Ⅱ)加热,产生大量红褐色沉淀,静置,上层溶液呈紫红色;
(Ⅲ)加入MnSO4至紫红色消失,过滤.
①步骤Ⅰ的目的:将Fe2+氧化为Fe3+;调节溶液的pH为3.7的目的是调节pH值使铁元素沉淀完全,此时溶液中c(Fe3+)为1.1×10-5.1mol•L-1
②向Ⅱ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是生成有黄绿色气体,写出其反应方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
③Ⅲ中加入MnSO4的目的是除去过量的MnO4-.
(4)从多次循环使用后母液中可回收的主要物质是K2SO4(填化学式)
16.下表是某地区市场上销售的一种“加碘食盐”包装袋上的部分文字说明.
该加碘食盐中添加的是KIO3(填化学式),根据图表中信息,可推测该添加物在受热时容易分解.
| 配料表 | 精制海盐.碘酸钾 |
| 含碘量 | 20~40mg/kg |
| 卫生许可证号 | ××卫碘字(2007)第005号 |
| 分装日期 | 见封底 |
| 储藏方法 | 密封.避光.防潮 |
| 食用方法 | 烹调时,待食品熟后加入碘盐 |
20.A、B、C、D、E是短周期的五种元素,原子序数依次增大,有关信息如下表所示.
填写下列空白.
(1)C元素为N.
(2)由上述两种元素组成的含有非极性键的一种化合物的化学式为H2O2等.
(3)A、B、C、D四种元素原子个数为7:2:1:2的离子化合物的化学式为CH3COONH4.
(4)由上述两种元素组成含有30个电子的阴离子,其钠盐水溶液呈碱性,理由是AlO2-+2H2O?Al(OH)3+OH-(用离子方程式表示).
| 元素 | 部分结构和性质 |
| A | 所有元素中原子半径最小 |
| B | 次外层电子数为最外层电子数的一半 |
| C | 单质由双原子分子构成,分子中有14个电子 |
| D | 地壳中含量最高的元素 |
| E | 最高价氧化物对应的水化物能溶于强酸和强碱 |
(1)C元素为N.
(2)由上述两种元素组成的含有非极性键的一种化合物的化学式为H2O2等.
(3)A、B、C、D四种元素原子个数为7:2:1:2的离子化合物的化学式为CH3COONH4.
(4)由上述两种元素组成含有30个电子的阴离子,其钠盐水溶液呈碱性,理由是AlO2-+2H2O?Al(OH)3+OH-(用离子方程式表示).
1.下列有关电解池的叙述不合理的是( )
| A. | 高温电解熔融氯化钠时,阴极得金属钠、阳极得氯气 | |
| B. | 工业电解饱和食盐水时,阴极区生成烧碱溶液和氢气、阳极得氯气 | |
| C. | 实验室用碳棒作电极电解氯化铜溶液时,在阴、阳极分别得到氯气和铜 | |
| D. | 镀锌时将两极材料浸入含锌离子的电解液中,锌棒接电源正极,待镀件接电源负极 |

 .
. 海水的综合利用可以制备金属镁,其流程如图所示:
海水的综合利用可以制备金属镁,其流程如图所示: