题目内容
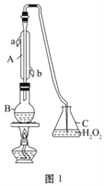
【题目】由NO2、O2、熔融盐NaNO3组成的燃料电池如图所示,在使用过程中石墨I电极反应生成一种氧化物Y,下列有关说法正确的是

A. 石墨I极为正极,石墨II极为负极
B. Y的化学式可能为NO
C. 石墨I极的电极反应式为NO2+NO3--e-=N2O5
D. 石墨II极上发生氧化反应
【答案】C
【解析】试题分析:A、燃料电池中通氧气的为正极,通燃料的为负极,则石墨I极为负极,石墨II极为正极,A错误;B、NO2中氮元素的化合价为+4价,反应后化合价升高,所以Y的化学式为N2O5,B错误;C、负极上NO2失电子生成N2O5,则石墨I极的电极反应式为NO2+NO3﹣﹣e﹣═N2O5,C正确;D、石墨II极为氧气得电子发生还原反应,D错误;故选C.

练习册系列答案
相关题目
【题目】下列相关实验能达到预期目的的是
相关实验 | 预期目的 | |
A | 用pH计测定NaF溶液和CH3COONa溶液可知,pH (NaF)<pH(CH3COONa) | 酸性 HF>CH3COOH |
B | 向一未知溶液中加入盐酸酸化的氯化钡溶液,生成大量白色沉淀 | 该溶液中一定含有SO42- |
C | 室温下,向BaSO4悬浊液中加入饱和Na2CO3溶液,过滤 后,再向沉淀中加入盐酸,沉淀部分溶解 | 可比较 BaSO4 和 BaCO3Kap 的相对大小 |
D | 其他条件相同,一只试管中加人5mL 0.2mol/LH2C2O2 (aq)和2.5L 0.1mol/LKMnO4(aq);另一支试管中加入7.5ml 0.2moI/LH2C2O4(aq)和 2.5mL 0.2mol/LKMnO4(aq) 和5mlH2O | 可验证相同条件下浓度对化学反应速率的影响 |
A. A B. B C. C D. D