题目内容
A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如图1所示(部分反应条件及产物略去).
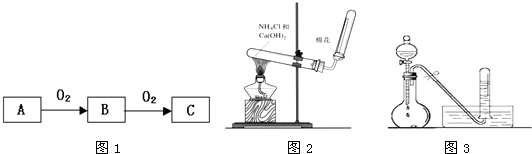
(1)若A是一种黄色单质固体,则B→C的化学方程式为
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为
(3)若C是红棕色气体,A可能是一种能使湿润的红色石蕊试纸变蓝的气体.如图2所示是实验室制取A气体的装置,请结合所学知识,回答下列问题:
①收集A的方法是
②写出实验室制取A的化学方程式
③若有5.35g氯化铵参加反应,则产生的A气体在标准状况下的体积为
④试写出C与水反应的化学方程式

(1)若A是一种黄色单质固体,则B→C的化学方程式为
2SO2+O2
2SO3
| 催化剂 |
| △ |
2SO2+O2
2SO3
.| 催化剂 |
| △ |
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为
过氧化钠
过氧化钠
,试用化学方程式表示该物质与二氧化碳气体的反应2Na2O2+2CO2=2Na2CO3+O2↑
2Na2O2+2CO2=2Na2CO3+O2↑
.将C长期露置于空气中,最后将变成物质D,D的化学式为Na2CO3
Na2CO3
.(3)若C是红棕色气体,A可能是一种能使湿润的红色石蕊试纸变蓝的气体.如图2所示是实验室制取A气体的装置,请结合所学知识,回答下列问题:
①收集A的方法是
向下排空气法
向下排空气法
,验证A是否已经收集满的方法是向下排空气法;将湿润的红色石蕊试纸置于试管口处,若试纸变蓝,则证明氨气已收集满;
(或用白色的酚酞试纸置于试管口处,若试纸变红,则证明氨气已收集满)
(或用蘸有浓盐酸的玻璃棒靠近试管口处,若产生大量白烟,则证明氨气已收集满)
(或用白色的酚酞试纸置于试管口处,若试纸变红,则证明氨气已收集满)
(或用蘸有浓盐酸的玻璃棒靠近试管口处,若产生大量白烟,则证明氨气已收集满)
向下排空气法;将湿润的红色石蕊试纸置于试管口处,若试纸变蓝,则证明氨气已收集满;
(或用白色的酚酞试纸置于试管口处,若试纸变红,则证明氨气已收集满)
(或用蘸有浓盐酸的玻璃棒靠近试管口处,若产生大量白烟,则证明氨气已收集满)
(任写一种).(或用白色的酚酞试纸置于试管口处,若试纸变红,则证明氨气已收集满)
(或用蘸有浓盐酸的玻璃棒靠近试管口处,若产生大量白烟,则证明氨气已收集满)
②写出实验室制取A的化学方程式
Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O
| ||
Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O
.
| ||
③若有5.35g氯化铵参加反应,则产生的A气体在标准状况下的体积为
2.24
2.24
L.④试写出C与水反应的化学方程式
3NO2+H2O=2HNO3+NO
3NO2+H2O=2HNO3+NO
,反应可得到酸X,X是强
强
电解质(填“强”或“弱”).如图3所示:足量X的浓溶液与Cu反应,写出烧瓶中发生反应的离子方程式Cu+4H++2NO3-=Cu2++2NO2↑+2H2O;
Cu+4H++2NO3-=Cu2++2NO2↑+2H2O;
.实验完毕后,试管中收集到的气体的主要成分为NO
NO
(写化学式)分析:(1)若A是一种黄色单质固体,则A是S单质,属于B是二氧化硫,C是三氧化硫;
(2)若A是一种活泼金属,C是淡黄色固体,则A是钠,B是氧化钠,C是过氧化钠;
(3)若A为能使湿润的红色石蕊试纸变蓝的气体,则A应该是氨气,C是红棕色气体,应为NO2.
(2)若A是一种活泼金属,C是淡黄色固体,则A是钠,B是氧化钠,C是过氧化钠;
(3)若A为能使湿润的红色石蕊试纸变蓝的气体,则A应该是氨气,C是红棕色气体,应为NO2.
解答:解:(1)若A是一种黄色单质固体,则A是S单质,属于B是二氧化硫,C是三氧化硫,则B→C的化学方程式为2SO2+O2
2SO3,故答案为:2SO2+O2
2SO3;
(2)若A是一种活泼金属,C是淡黄色固体,则A是钠,B是氧化钠,C是过氧化钠.过氧化钠能吸收CO2生成氧气,反应的化学方程式是2Na2O2+2 CO2=2 Na2CO3+O2↑,
故答案为:过氧化钠; 2Na2O2+2 CO2=2 Na2CO3+O2↑;Na2CO3;
(3)若A为能使湿润的红色石蕊试纸变蓝的气体,则A应该是氨气,C是红棕色气体,应为NO2,
①A为氨气,极易溶于水,密度比空气小,可用向下排空气法收集,检验氨气是否收集满,可将湿润的红色石蕊试纸置于试管口处,若试纸变蓝,则证明氨气已收集满,或用白色的酚酞试纸置于试管口处,若试纸变红,则证明氨气已收集满,也可以用蘸有浓盐酸的玻璃棒靠近试管口处,若产生大量白烟,则证明氨气已收集满,
故答案为:向下排空气法;将湿润的红色石蕊试纸置于试管口处,若试纸变蓝,则证明氨气已收集满;
(或用白色的酚酞试纸置于试管口处,若试纸变红,则证明氨气已收集满)
(或用蘸有浓盐酸的玻璃棒靠近试管口处,若产生大量白烟,则证明氨气已收集满)
②实验室用氢氧化钙和氯化铵在加热条件下反应准备氨气,反应的方程式为Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O,
故答案为:Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O;
③n(NH4Cl)=
=0.1mol,则n(NH3)=0.1mol,V(NH3)=2.24L,
故答案为:2.24;
④C为NO2,与水反应生产硝酸和NO,反应的方程式为3NO2+H2O=2HNO3+NO,HNO3是强电解质,具有强氧化性,可用铜反应,反应的离子方程式为Cu+4H++2NO3-=Cu2++2NO2↑+2H2O,实验完毕后,试管中收集到的气体的主要成分为NO.
故答案为:3NO2+H2O=2HNO3+NO;强;Cu+4H++2NO3-=Cu2++2NO2↑+2H2O;NO.
| 催化剂 |
| △ |
| 催化剂 |
| △ |
(2)若A是一种活泼金属,C是淡黄色固体,则A是钠,B是氧化钠,C是过氧化钠.过氧化钠能吸收CO2生成氧气,反应的化学方程式是2Na2O2+2 CO2=2 Na2CO3+O2↑,
故答案为:过氧化钠; 2Na2O2+2 CO2=2 Na2CO3+O2↑;Na2CO3;
(3)若A为能使湿润的红色石蕊试纸变蓝的气体,则A应该是氨气,C是红棕色气体,应为NO2,
①A为氨气,极易溶于水,密度比空气小,可用向下排空气法收集,检验氨气是否收集满,可将湿润的红色石蕊试纸置于试管口处,若试纸变蓝,则证明氨气已收集满,或用白色的酚酞试纸置于试管口处,若试纸变红,则证明氨气已收集满,也可以用蘸有浓盐酸的玻璃棒靠近试管口处,若产生大量白烟,则证明氨气已收集满,
故答案为:向下排空气法;将湿润的红色石蕊试纸置于试管口处,若试纸变蓝,则证明氨气已收集满;
(或用白色的酚酞试纸置于试管口处,若试纸变红,则证明氨气已收集满)
(或用蘸有浓盐酸的玻璃棒靠近试管口处,若产生大量白烟,则证明氨气已收集满)
②实验室用氢氧化钙和氯化铵在加热条件下反应准备氨气,反应的方程式为Ca(OH)2+2NH4Cl
| ||
故答案为:Ca(OH)2+2NH4Cl
| ||
③n(NH4Cl)=
| 5.35g |
| 53.5g/mol |
故答案为:2.24;
④C为NO2,与水反应生产硝酸和NO,反应的方程式为3NO2+H2O=2HNO3+NO,HNO3是强电解质,具有强氧化性,可用铜反应,反应的离子方程式为Cu+4H++2NO3-=Cu2++2NO2↑+2H2O,实验完毕后,试管中收集到的气体的主要成分为NO.
故答案为:3NO2+H2O=2HNO3+NO;强;Cu+4H++2NO3-=Cu2++2NO2↑+2H2O;NO.
点评:该题考查无机框图题的判断,是高考中的常见题型,属于基础性试题的考查.试题难易适中,基础知识,侧重对学生基础知识的巩固个训练.该类试题需要注意的是化学推断题是一类综合性较强的试题,如元素及化合物性质和社会生活,环境保护,化学计算等知识,还可引入学科间综合.它不仅可考查学生对化学知识的理解程度,更重要的是培养学生的综合分析能力和思维方法.解框图题的方法:最关键的是寻找“突破口”,“突破口”就是抓“特”字,例如特殊颜色、特殊状态、特殊气味、特殊反应、特殊现象、特殊制法、特殊用途等.

练习册系列答案
相关题目



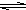 HS-+OH-
HS-+OH-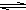 Al(OH)3+3H+有无色气体和白色絮状沉淀产生
Al(OH)3+3H+有无色气体和白色絮状沉淀产生 已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系:
已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系: