题目内容
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,3.20gN2H4在氧气中完全燃烧生成氮气,放出热量62.4kJ(25℃时),N2H4完全燃烧反应的热化学方程式是 。
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时:正极的电极反应式是 。负极的电极反应式是 _ _。
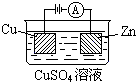
(3)下图是一个电化学过程示意图。
①锌片上发生的电极反应是 。
②假设使用肼—空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼一空气燃料电池理论上消耗标标准状况下的空气 L(假设空气中氧气体积含量为20%)。
(4)传统制备肼的方法是以NaClO氧化NH3,制得肼的稀溶液。该反应的离子方程式是 。
(1)N2H4(1)+O2(g)=N2(g)+2H2O(1);△H=-624kJ/mol(3分)
(2)O2+2H2O+4e-=4OH- ;(2分) N2H4+4OH--4e-=4H2O+N2↑(2分)
(3)①Cu2++2e-=Cu (2分) ②112(2分)
(4)ClO-+2NH3=N2H4+Cl-+H2O(2分)
解析:略

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

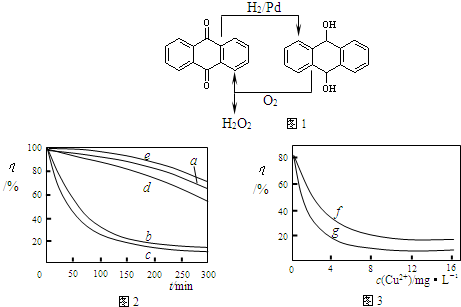
 (1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是