题目内容
(8分)A、B、C三元素原子的核外电子数都比氩原子少, A和C处于同主族,两者间隔一周期, A元素和B元素的原子两者核电荷数之差为5, B原子核外第3电子层比第2电子层少两个电子,则B的原子结构示意图为______;A离子的结构示意图为_____;B与C形成化合物的化学式是_____,它的电子式是 它属于 化合物(填“离子”或“共价”);A与B形成化合物的化学式是 ,它的电子式是 ,它属于 化合物。
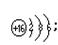 ;
;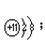 ; H2S,
; H2S,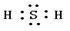 共价; Na2S ,
共价; Na2S ,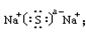 离子 。
离子 。考查原子核外电子的排布规律、元素周期表的结构以及化学键的判断。B原子核外第3电子层比第2电子层少两个电子,则B是硫元素,所以A是钠元素,C就是氢元素。硫和氢形成的化学键是极性键,化合物是共价化合物。钠是活泼的金属,和硫形成离子键,化合物是离子化合物。

练习册系列答案
相关题目
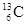 -NMR(核磁共振)可用于含碳化合物的结构分析,
-NMR(核磁共振)可用于含碳化合物的结构分析,