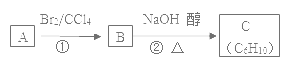题目内容
【题目】根据下面的反应路线及所给信息填空。
(1)A的名称是________________ ;B的分子式为______________。
(2)反应①的方程式为:________________;反应②为_______________反应;反应④的化学方程式是__________________。
(3)写出B在NaOH水溶液中加热的反应方程式:_____________,生成物官能团的名称为__________。
【答案】环己烷 C6H11Cl ![]() +Cl2
+Cl2![]()
![]() +HCl 消去反应
+HCl 消去反应 ![]() +2NaOH
+2NaOH![]()
![]() +2NaBr+2H2O
+2NaBr+2H2O ![]() +NaOH
+NaOH![]()
![]() +NaCl 羟基
+NaCl 羟基
【解析】
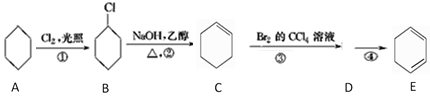
A是环己烷,与Cl2在光照时发生取代反应产生一氯环己烷,该物质与NaOH的乙醇溶液在加热时发生消去反应产生环己烯![]() ,环己烯与溴的四氯化碳溶液发生加成反应生成
,环己烯与溴的四氯化碳溶液发生加成反应生成![]() (物质D),
(物质D),![]() 与NaOH的乙醇溶液在加热时发生消去反应产生环己二烯
与NaOH的乙醇溶液在加热时发生消去反应产生环己二烯![]() ,据此分析解答。
,据此分析解答。
(1)碳原子结合形成环状,每个碳原子结合的H原子数达到最大数目,由于环上有6个C原子,所以可知A的名称为环己烷,A的分子式是C6H12;B的结构简式为![]() ,B的分子式为C6H11Cl;
,B的分子式为C6H11Cl;
(2)反应①是环己烷与氯气发生的取代反应,方程式为:![]() +Cl2
+Cl2![]()
![]() +HCl;反应②为一氯环己烷与NaOH的乙醇溶液发生消去反应生成环己烯及NaBr、H2O;环己烯与溴的四氯化碳溶液发生加成反应生成1,2-二溴环己烷(物质D),由于两个Br原子连接的C原子的邻位C原子上有H原子,所以1,2-二溴环己烷与NaOH的乙醇溶液发生消去反应生成环己二烯及NaBr、H2O,所以反应④的化学方程式是
+HCl;反应②为一氯环己烷与NaOH的乙醇溶液发生消去反应生成环己烯及NaBr、H2O;环己烯与溴的四氯化碳溶液发生加成反应生成1,2-二溴环己烷(物质D),由于两个Br原子连接的C原子的邻位C原子上有H原子,所以1,2-二溴环己烷与NaOH的乙醇溶液发生消去反应生成环己二烯及NaBr、H2O,所以反应④的化学方程式是![]() +2NaOH
+2NaOH![]()
![]() +2NaBr+2H2O;
+2NaBr+2H2O;
(3) B是![]() ,属于氯代烃,在NaOH水溶液中加热发生取代反应生成环己醇,该反应方程式:
,属于氯代烃,在NaOH水溶液中加热发生取代反应生成环己醇,该反应方程式:![]() +NaOH
+NaOH![]()
![]() +NaCl,生成物
+NaCl,生成物![]() 的官能团是—OH,名称为羟基。
的官能团是—OH,名称为羟基。