题目内容
16.能正确表示下列反应的离子方程式为( )| A. | 硫化亚铁溶于稀硝酸中:FeS+2 H+═Fe2++H2S↑ | |
| B. | NH4HCO3溶于过量NaOH溶液中:HCO3-+OH-═CO32-+H2O | |
| C. | 少量二氧化碳通入苯酚钠溶液中:C6H5O-+CO2+H2O═C6H5OH+CO32- | |
| D. | 大理石溶于醋酸中:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O |
分析 A.硫化亚铁具有还原性,而硝酸具有氧化性,两者要发生氧化还原反应;
B.NH4HCO3溶于过量NaOH溶液中生成碳酸钠和氨气;
C.少量二氧化碳通入苯酚钠溶液中生成苯酚和碳酸氢钠;
D.大理石不溶于水,醋酸为弱酸,应写成化学式,二者反应生成醋酸钙、水和二氧化碳.
解答 解:A.硫化亚铁具有还原性,而硝酸具有氧化性,两者要发生氧化还原反应,正确的离子反应为FeS+4H++NO3-=Fe3++S↓+NO↑+2H2O,故A错误;
B.NH4HCO3溶于过量NaOH溶液中生成碳酸钠和氨气,反应的离子方程式为NH4++HCO3-+2OH-═CO32-+2H2O+NH3↑,故B错误;
C.向苯酚钠溶液中通入少量CO2气体生成苯酚和碳酸氢钠,反应的离子方程式为C6H5O-+CO2+H2O═C6H5OH+HCO3-,故C错误;
D.大理石不溶于水,醋酸为弱酸,应写成化学式,二者反应生成醋酸钙、水和二氧化碳,反应的离子方程式为CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O,故D正确.
故选D.
点评 本题考查了离子方程式的判断,为中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
17.现有下列有机化合物:
①CH3CH2CH2CH2CH3
②CH3CH2CH2OH
③CH3CH2CH3
④CH3CHBrCH3
⑤(CH3)2-CH-CH=CH-CH3
⑥
⑦CH2OH-CHOH-CH2OH
⑧(CH3)2-CH-COOH
⑨CH3CH2CH2CHO
请你按要求对以上有机化合物进行分类,并把正确答案的序号填入下表中:
①CH3CH2CH2CH2CH3
②CH3CH2CH2OH
③CH3CH2CH3
④CH3CHBrCH3
⑤(CH3)2-CH-CH=CH-CH3
⑥

⑦CH2OH-CHOH-CH2OH
⑧(CH3)2-CH-COOH
⑨CH3CH2CH2CHO
请你按要求对以上有机化合物进行分类,并把正确答案的序号填入下表中:
| 烷烃 | 烯烃 | 芳香烃 | 卤代烃 | 醇 | 醛 | 羧酸 | 脂肪烃 |
| ①③ | ⑤ | ⑥ | ④ | ②⑦ | ⑨ | ⑧ | ①③⑤ |
7.金刚石和石墨是碳元素的两种结构不同的单质(同素异形体).在100kPa时,1mol石墨转化为金刚石,要吸收1.895kJ的热能.据此,试判断在100kPa压强下,下列结论正确的是( )
| A. | 石墨比金刚石稳定 | |
| B. | 金刚石比石墨稳定 | |
| C. | 1mol石墨比1 mol金刚石的总能量高 | |
| D. | 1mol石墨比1 mol金刚石的总能量低 |
11.用已知浓度的盐酸进行滴定未知浓度的NaOH溶液,下列情况可能引起测定结果偏高的是( )
| A. | 滴定终点时俯视读数 | |
| B. | 滴定前滴定管尖嘴中有一气泡,滴定后气泡消失了 | |
| C. | 锥形瓶未用待测液润洗 | |
| D. | 滴定前,滴定管中的溶液液面最低点未定在“0”点 |
8.下列实验操作可以达到实验目的是( )
| 实验目的 | 实验操作 | |
| A | 验证乙烯能被酸性高锰酸钾溶液氧化 | 将乙醇与浓硫酸反应生成的气体通往酸性高锰酸钾溶液,观察溶液是否褪色 |
| B | 检验淀粉水解产物的还原性 | 取少量淀粉溶液,与稀硫酸共热后再加入银氨溶液,水浴加热,观察是否出现银镜 |
| C | 检验溴乙烷中的溴元素 | 取少量溴乙烷,与氢氧化钠溶液共热后加入硝酸银溶液,观察是否出现浅黄色沉淀 |
| D | 证明溴乙烷发生消去反应有乙烯生成 | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反应产生的气体先通过盛有水的洗气瓶再通入酸性高锰酸钾溶液 |
| A. | A | B. | B | C. | C | D. | D |
5.下列物质在一定条件下能够导电,但是不属于电解质的是( )
| A. | 铜 | B. | 食盐 | C. | 硫酸 | D. | 酒精 |
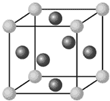 氯化铬酰(CrO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应.请回答下列问题:
氯化铬酰(CrO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应.请回答下列问题: