题目内容
13.下列反应中,既属于氧化还原反应,又是吸热反应的是( )| A. | NaOH与HCl的反应 | B. | 灼热的碳与二氧化碳的反应 | ||
| C. | Ba(OH)2•8H2O与NH4Cl的反应 | D. | 酒精在空气中的燃烧反应 |
分析 存在元素的化合价变化的反应为氧化还原反应,常见的吸热反应有:Ba(OH)2•8H2O与NH4Cl反应、大多数的分解反应、C(或氢气)参加的氧化还原反应等,以此来解答.
解答 解:A、酸碱中和反应为放热反应,没有元素化合价变化,不属于氧化还原反应,故A不选;
B、灼热的碳与二氧化碳的反应为吸热反应,且C元素的化合价变化,属于氧化还原反应,故B选;
C、Ba(OH)2•8H2O与NH4Cl反应为吸热反应,没有元素化合价变化,不属于氧化还原反应,故C不选;
D、酒精在空气中的燃烧反应为放热反应,属于氧化还原反应,故D不选,
故选B.
点评 本题考查氧化还原反应,侧重反应类型判断的考查,注意化合价角度及归纳常见的吸热反应分析,题目难度不大.

练习册系列答案
相关题目
3.25℃时,向10ml0.01mol/LKOH溶液中滴加0.01mol/L苯酚溶液,混合溶液中粒子浓度关系正确的( )
| A. | pH>7时,c(C6H5O-)>c(K+)>c(H+)>c(OH-) | |
| B. | pH<7时,c(K+)>c(C6H5O-)>c(H+)>c(OH-) | |
| C. | V[C6H5OH(aq)]=20ml时,c(C6H5O-)+c(C6H5OH)=2c(K+) | |
| D. | V[C6H5OH(aq)]=10ml时,c(K+)=c(C6H5O-)>c(OH-)=c(H+) |
4.关于元素周期表,下列叙述中不正确的是( )
| A. | 在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素 | |
| B. | 在过渡元素中可以寻找制备催化剂及耐高温和耐腐蚀的元素 | |
| C. | 在金属元素区域可以寻找制备新型农药材料的元素 | |
| D. | 过渡元素是副族和第Ⅷ族元素的总称 |
1.N2O5是一种新型硝化剂,其性质和制备受到人们的关注.一定温度下,在2L固定容积的密闭容器中发生反应:2N2O5(g)?4NO2(g)+O2(g)△H>0,反应物和部分生成物的物质的量随反应时间变化的曲线如图所示,下列说法中不正确的是( )
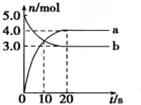

| A. | 曲线a表示NO2的物质的量随时间的变化 | |
| B. | 10s时,v(正)>v(逆) | |
| C. | 20s时反应达到平衡 | |
| D. | 0~20s内平均反应速率v(O2)=0.05mol•L-1•s-1 |
8.X元素最高价氧化物对应的水化物为HXO3,其气态氢化物为( )
| A. | HX | B. | XH3 | C. | H2X | D. | XH4 |
18.酸和醇可以发生酯化反应,生成酯类物质,下列酸和醇能生成相对分子质量为90的酯的是( )
| A. | CH3C18OOH与C2H518OH | B. | CH3C18O18OH与C2H518OH | ||
| C. | CH3CO18OH与C2H518OH | D. | CH3CO18OH 与C2H5OH |
5.根据如表推断下列说法中不正确的是( )
| 性质 | 金刚石 | 石墨 |
| 外观 | 无色,透明固体 | 灰黑,不透明固体 |
| 沸点 | ? | ? |
| 熔点 | ? | ? |
| 燃烧热/kJ•mol-1 | 395.4 | 393.5 |
| A. | C(石墨,s)═C(金刚石,s)△H=+1.9kJ•mol-1 | |
| B. | 在相同条件下石墨的熔点应高于金刚石 | |
| C. | 金刚石中碳碳键键能大于石墨中碳碳键键能 | |
| D. | 在相同条件下石墨和金刚石的沸点应相同 |
2.下列化学用语描述中不正确的是( )
| A. | 中子数为20的氯原子: | |
| B. | K2O的电子式: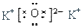 | |
| C. | HCO3-的电离方程式:HCO3-+H2O?CO32-+H3O+ | |
| D. | 比例模型 可以表示CO2分子或SiO2 可以表示CO2分子或SiO2 |
3.用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 标准状况下,22.4L CCl4含有的分子数为NA | |
| B. | 2.4gMg溶于足量稀盐酸,转移的电子数为0.1NA | |
| C. | 通常状况下,32gO2与32gO3所含的氧原子数均为2NA | |
| D. | 质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 的数目为NA |