题目内容
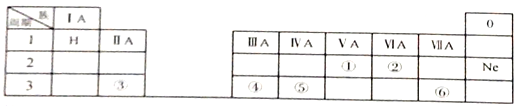
【题目】A、B、C、D、E、 F、G是周期表中短周期的七种元素,有关性质或结构信息如下表:
元素 | 有关性质或结构信息 |
A | 地壳中含量最多的元素 |
B | B阳离子与A阴离子电子数相同,且是所在周期中单核离子半径最小的 |
C | C与B同周期,且是所在周期中原子半径最大的(稀有气体除外) |
D | D原子最外层电子数是电子层数的2倍,其氢化物有臭鸡蛋气味 |
E | E与D同周期,且在该周期中原子半径最小 |
F | F的氢化物和最高价氧化物的水化物反应生成一种离子化合物 |
G | G是形成化合物种类最多的元素 |
(1) B元素符号为____,A与C以原子个数比为1:1形成的化合物的电子式为___,用电子式表示C与E形成化合物的过程____, D形成的简单离子的结构示意图为____。
(2) F的氢化物是由____(极性或非极性)键形成的分子,写出实验室制备该氢化物的化学方程式____。
(3) 非金属性D____E(填大于或小于),请从原子结构的角度解释原因:__。
【答案】 Al ![]()
![]()
![]() 极性 2NH4Cl+ Ca(OH)2
极性 2NH4Cl+ Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O 小于 D的原子半径大于E的原子半径,所以得电子的能力比E弱
CaCl2+2NH3↑+2H2O 小于 D的原子半径大于E的原子半径,所以得电子的能力比E弱
【解析】A是地壳中含量最多的元素,则A为O元素;B阳离子与A离子电子数相同,且是所在周期中单核离子半径最小的,则B为Al;C与B同周期,且是所在周期中原子半径最大的(稀有气体除外),则C为Na;D原子最外层电子数是电子层数的2倍,其氢化物有臭鸡蛋气味,则D为S元素;E与D同周期,且在该周期中原子半径最小,则E为Cl;F的氢化物和最高价氧化物的水化物反应生成一种离子化合物,则F为N元素;G是形成化合物种类最多的元素,则G为碳元素;
(1) 由分析可知B元素符号为Al,O与Na以原子个数比为1:1形成的离子化合物Na2O2的电子式为![]() ;离子化合NaCl的电子式形成过程为
;离子化合NaCl的电子式形成过程为![]() , S2-的离子的结构示意图为
, S2-的离子的结构示意图为![]() ;
;
(2) NH3是由极性键形成的极性分子,实验室利用氯化铵和氢氧化钙混合加热制备氨气的化学方程式为2NH4Cl+ Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O;
CaCl2+2NH3↑+2H2O;
(3)S的原子半径大于Cl的原子半径,所以S得电子的能力比Cl弱 ,即S元素的非金属性小于Cl的非金属性。

 轻松暑假总复习系列答案
轻松暑假总复习系列答案