题目内容
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.标准状况下,33.6L HF中含有氟原子的数目为1.5NA |
| B.常温常压下,9.2g二氧化氮和四氧化二氮的混合物含有氮原子的数目为0.2NA |
| C.50mL18.4mol·L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA |
| D.0.1mol铁溶于足量氯水中,转移电子的总数为0.2NA |
解析试题分析:A选项,标准状态下,HF为液态,故不能用气体公式计算,错误。B选项,N2O4=2(NO2),故9.2g二氧化氮和四氧化二氮的混合物相当于含有9.2gNO2或N2O4,故含有N原子数目为0.2NA,B正确。C选项,18.4mol·L-1浓硫酸,当反应一段时间后浓度变低,不再发生反应,故不能完全反应,生成SO2分子的数目小于0.46NA。C错误。D选项,由于氯水中含有次氯酸,具有强氧化性,能够将二价铁离子氧化为三价铁离子,故转移电子数为0.3NA。D错误。
考点:阿伏伽德罗常数

练习册系列答案
相关题目
下列化学用语书写正确的是( )
| A.中子数为10的氧原子:108O |
| B.亚硫酸铵的化学式:(NH3) 2SO3 |
| C.碳酸钾的电离方程式:K2CO3=2K+1 + CO3-2 |
D.硫离子的结构示意图为: |
相同质量的SO2和SO3它们之间的关系正确的是( )
| A.所含硫原子的物质的量之比为1:1 | B.氧原子的物质的量之比为5:6 |
| C.氧元素的质量比为2:3 | D.硫元素的质量比为5:4 |
化学用语是学习化学的重要工具。下列化学用语错误的是 ( )
A.碳酸钠的水解反应:CO32-+H2O 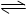 HCO3-+OH- HCO3-+OH- |
B.FeCl3水解的离子方程式:Fe3++3H2O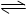 Fe (OH)3+3H+ Fe (OH)3+3H+ |
| C.稀溶液中强酸与强碱的中和热:H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3 kJ· mol-1 |
| D.C燃烧的热化学方程式为:C(s)+1/2O2(g)=CO(g)△H = 110.5kJ·mol-1 |
下列各组物质中,分子数目相同的是
| A.2g H2和16gO2 |
| B.1 mol O2和18gH2O |
| C.22.4 L He和1mol H2 |
| D.标准状况下,2 L H2和2 L H2O |
设NA为阿伏加德罗常数的值,下列说法中正确的是
| A.62 g Na2O溶液于水后所得溶液中含有的O2-数为NA |
| B.标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA |
| C.常温常压下,16g甲烷(12C1H)所含的中子数为10NA |
| D.常温常压下,14g由N2和CO组成的混合气体含有的原子数目为NA |
过量的硝酸和6.4g铜充分反应,向反应后的溶液中滴加5 mol·L-1的氢氧化钠溶液,加入氢氧化钠溶液的体积与生成沉淀的关系如图所示,则反应后溶液中所含NO3-的物质的量为
| A.0.05mol | B.0.1mol |
| C.0.2mol | D.0.25mol |
以色列科学家Daniel Shechtman因发现准晶体获得2011年诺贝尔化学奖。人们在自然界中也找到了组成为Al63Cu24Fe13的天然准晶体。将相同质量的此准晶体分别与足量的盐酸、烧碱和稀硝酸反应,产生气体的物质的量关系为
| A.n(烧碱)<n(稀硝酸)<n(盐酸) | B.n(烧碱)<n(盐酸)<n(稀硝酸) |
| C.n(稀硝酸)<n(烧碱)<n(盐酸) | D.n(盐酸)<n(稀硝酸)<n(烧碱) |
下列叙述正确的是
| A.摩尔是国际上规定的七个基本物理量之一 |
| B.不同的气体,若体积不等,则它们所含的分子数一定不等 |
| C.一定温度、压强下,各种气态物质分子间距离近似相等 |
| D.气体的摩尔体积为22.4L/mol |