题目内容
元素X、Y、Z的原子序数都小于18,X的阳离子,Y的阳离子和Z的阴离子都具有相同的电子层结构,Y的阳离子半径小于X的阳离子半径,则元素X、Y、Z的原子序数由小到大的顺序依次是( )
| A、Z、Y、X |
| B、Y、Z、X |
| C、Y、X、Z |
| D、Z、X、Y |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:核外电子排布相同,核电荷数越大,离子半径越小.
X元素的阳离子、Y元素的阳离子和Z元素的阴离子具有相同的电子层结构.X元素、Y元素形成阳离子,则X、Y两元素处于同一周期.Z元素形成阴离子,则Z元素位于X、Y元素所在周期的相邻上一周期,以此解答该题.
X元素的阳离子、Y元素的阳离子和Z元素的阴离子具有相同的电子层结构.X元素、Y元素形成阳离子,则X、Y两元素处于同一周期.Z元素形成阴离子,则Z元素位于X、Y元素所在周期的相邻上一周期,以此解答该题.
解答:
解:核外电子排布相同,核电荷数越大,离子半径越小.
X元素的阳离子、Y元素的阳离子和Z元素的阴离子具有相同的电子层结构.X元素、Y元素形成阳离子,则X、Y两元素处于同一周期.Z元素形成阴离子,则Z元素位于X、Y元素所在周期的相邻上一周期,
所以Z的原子半径最小,核外电子排布相同,核电荷数越大,离子半径越小.X的阳离子半径大于Y的阳离子半径,则X的原子序数小于Y,则原子序数大小关系为Z<X<Y,
故选D.
X元素的阳离子、Y元素的阳离子和Z元素的阴离子具有相同的电子层结构.X元素、Y元素形成阳离子,则X、Y两元素处于同一周期.Z元素形成阴离子,则Z元素位于X、Y元素所在周期的相邻上一周期,
所以Z的原子半径最小,核外电子排布相同,核电荷数越大,离子半径越小.X的阳离子半径大于Y的阳离子半径,则X的原子序数小于Y,则原子序数大小关系为Z<X<Y,
故选D.
点评:本题考查了元素的位置、结构和性质的关系,为高考常见题型,难度不大,关键根据离子具有相同的电子层结构推断元素的相对位置.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在空气中放置,因发生氧化还原反应而变质的是( )
| A、Na |
| B、Na2O |
| C、Na2CO3 |
| D、NaOH |
在无色透明的溶液中能大量共存的是( )
| A、HCO3-、Na+、OH-、Cl- |
| B、Ca2+、NO3-、SO42-、CO32- |
| C、Fe2+、Na+、H+、NO3- |
| D、Cl-、Mg2+、Na+、SO42- |
把6molA气体和5molB气体混合放入4L密闭容器中,在一定条件下发生反应:3A(g)+B(g)?2C(g)+xD(g),经5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1mol/(L?min),下列说法错误的是( )
| A、x=2 |
| B、B的转化率为20% |
| C、平衡时A的浓度为0.8mol/L |
| D、恒温达平衡时容器内的压强与开始时相等 |
下列实验设计及其对应的离子方程式均正确的是( )
| A、NaHSO4与NaOH溶液反应:H++OH-=H2O |
| B、少量的Fe与稀硝酸反应:Fe+2H+=Fe2++H2↑ |
| C、实验室利用氢氧化钙固体和氯化铵反应制备氨气:NH4++OH-=NH3↑+H2O |
| D、金属Na与水反应:Na+H2O=Na++OH-+H2↑ |
苯分子中不存在碳碳单、双键的交替结构,下列可以作为证据的事实是( )
①苯不能使酸性KMnO4溶液褪色
②苯不能因发生化学反应而使溴的四氯化碳溶液褪色
③苯在加热和有催化剂存在的条件下能与H2加成生成环已烷
④苯分子中碳碳键长完全相等
⑤邻二氯苯( )只有一种
)只有一种
⑥间二氯苯(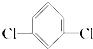 )只有一种.
)只有一种.
①苯不能使酸性KMnO4溶液褪色
②苯不能因发生化学反应而使溴的四氯化碳溶液褪色
③苯在加热和有催化剂存在的条件下能与H2加成生成环已烷
④苯分子中碳碳键长完全相等
⑤邻二氯苯(
 )只有一种
)只有一种⑥间二氯苯(
 )只有一种.
)只有一种.| A、①② | B、①⑤ |
| C、③④⑤⑥ | D、①②④⑤ |
某溶液中含有NH4+、Mg2+、Fe2+、Al3+、SO42-五种离子,若向其中加入过量的氢氧化钡溶液,微热并搅拌,再加入过量的氢碘酸,溶液中大量减少的离子有( )
| A、4 种 |
| B、3 种 |
| C、2 种 |
| D、1 种 |