题目内容
【题目】过二硫酸钾(K2S2O8) 在科研与工业上有重要用途。
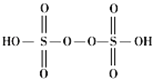
(1)H2S2O8的结构式如图,其中S元素的化合价为__________。在Ag+催化下,S2O82-能使含Mn2+的溶液变成紫红色,氧化产物是___________(填离子符号)。
(2)某厂采用湿法K2S2O8氧化脱硝和氨法脱硫工艺综合处理锅炉烟气,提高了烟气处理效率,处理液还可以用作城市植被绿化的肥料。
①脱硫过程中,当氨吸收液的pH=6时,n(SO32-)∶n(HSO3-)=________。
[巳知:25℃时,Ka1(H2SO3)=1.5×10-2,K a2(H2SO3)=1.0×10-7]
②脱硝过程中依次发生两步反应:第1步,K2S2O8将NO氧化成HNO2,第2步,K2S2O8继续氧化HNO2,第2步反应的化学方程式为______________________________________;
(3)过二硫酸钾可通过“电解→转化→提纯”方法制得,电解装置示意图如图所示。
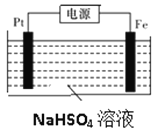
①电解时,铁电极连接电源的_________________极。
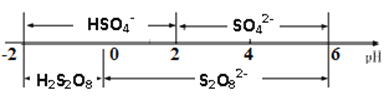
②常温下,电解液中含硫微粒的主要存在形式与pH的关系如下图所示。在阳极放电的离子主要是HSO4-,阳极区电解质溶液的pH范围为_________,阳极的电极反应式为________________________。
③往电解产品中加入硫酸钾,使其转化为过二硫酸钾粗产品,提纯粗产品的方法____。
【答案】+6 MnO4- 1:10 HNO2+K2S2O8+H2O=HNO3+K2SO4+H2SO4 负 0—2 2HSO4--2e-= S2O82-+2H+ 重结晶
【解析】
(1)过二硫酸结构简式为 ,存在1个过氧键(-O-O-)、4个S=O键,4个S-O键,4个S=O键中,4个O原子显-2价、过氧键(-O-O-)2个O原子显-1价,4个S-O键中4个O原子显-2价,根据化合价代数和等于0计算硫元素的化合价;过二硫酸中含有-1价氧原子,所以过二硫酸具有氧化性,S2O82-能使含Mn2+的溶液变成紫红色,说明有MnO4-生成;(2)①根据K a2(H2SO3)=
,存在1个过氧键(-O-O-)、4个S=O键,4个S-O键,4个S=O键中,4个O原子显-2价、过氧键(-O-O-)2个O原子显-1价,4个S-O键中4个O原子显-2价,根据化合价代数和等于0计算硫元素的化合价;过二硫酸中含有-1价氧原子,所以过二硫酸具有氧化性,S2O82-能使含Mn2+的溶液变成紫红色,说明有MnO4-生成;(2)①根据K a2(H2SO3)=![]() 计算pH=6时,n(SO32-)∶n(HSO3-)的值;②亚硝酸被氧化为硝酸, S2O82-被还原为SO42-;(3)①NaHSO4溶液制取过二硫酸钾,氧元素失电子发生氧化反应,若铁作阳极,则铁失电子发生氧化反应;②根据阳极放电的离子是HSO4-,电解产物是Na2S2O8分析;根据溶解度不同提纯提纯粗产品;
计算pH=6时,n(SO32-)∶n(HSO3-)的值;②亚硝酸被氧化为硝酸, S2O82-被还原为SO42-;(3)①NaHSO4溶液制取过二硫酸钾,氧元素失电子发生氧化反应,若铁作阳极,则铁失电子发生氧化反应;②根据阳极放电的离子是HSO4-,电解产物是Na2S2O8分析;根据溶解度不同提纯提纯粗产品;
(1)过二硫酸结构简式为 ,存在1个过氧键(-O-O-)、4个S=O键,4个S-O键,4个S=O键中,4个O原子显-2价、过氧键(-O-O-)2个O原子显-1价,4个S-O键中4个O原子显-2价,根据化合价代数和等于0,硫元素的化合价为+6;过二硫酸中含有-1价氧原子,所以过二硫酸具有氧化性,S2O82-能使含Mn2+的溶液变成紫红色,说明有MnO4-生成,所以氧化产物是MnO4-;(2)①根据K a2(H2SO3)=
,存在1个过氧键(-O-O-)、4个S=O键,4个S-O键,4个S=O键中,4个O原子显-2价、过氧键(-O-O-)2个O原子显-1价,4个S-O键中4个O原子显-2价,根据化合价代数和等于0,硫元素的化合价为+6;过二硫酸中含有-1价氧原子,所以过二硫酸具有氧化性,S2O82-能使含Mn2+的溶液变成紫红色,说明有MnO4-生成,所以氧化产物是MnO4-;(2)①根据K a2(H2SO3)=![]() , pH=6时,
, pH=6时,![]()
![]() ,所以n(SO32-)∶n(HSO3-)=1:10;②亚硝酸被氧化为硝酸, S2O82-被还原为SO42-,反应方程式为HNO2+K2S2O8+H2O=HNO3+K2SO4+H2SO4 ;(3)①NaHSO4溶液制取过二硫酸钾,氧元素失电子发生氧化反应,若铁作阳极,则铁失电子发生氧化反应,所以铁作阴极,连接电源负极;②根据图示,阳极放电的离子是HSO4-,电解产物是Na2S2O8,所以控制pH的范围是0—2;阳极的电极反应式为2HSO4--2e-= S2O82-+2H+;③提纯过二硫酸钾的方法是重结晶。
,所以n(SO32-)∶n(HSO3-)=1:10;②亚硝酸被氧化为硝酸, S2O82-被还原为SO42-,反应方程式为HNO2+K2S2O8+H2O=HNO3+K2SO4+H2SO4 ;(3)①NaHSO4溶液制取过二硫酸钾,氧元素失电子发生氧化反应,若铁作阳极,则铁失电子发生氧化反应,所以铁作阴极,连接电源负极;②根据图示,阳极放电的离子是HSO4-,电解产物是Na2S2O8,所以控制pH的范围是0—2;阳极的电极反应式为2HSO4--2e-= S2O82-+2H+;③提纯过二硫酸钾的方法是重结晶。