题目内容
(10分)A,B,C,D是四种短周期元素,它们的原子序数依次增大,其中A,C及B,D分别是同一主族元素,B,D元素的原子核中质子数之和是A,C两元素原子核中质子数之和的两倍,又知四种元素的单质中有两种气体、两种固体.
(1)写出四种元素的名称:
A_________;B_________;C_________;D_________;
(2)写出两种均含A,B,C,D四种元素的化合物相互间发生反应,且生成气体的离子方程式____________________________________________________;
(3)写出C和D两元素形成化合物的电子式:_________________________;
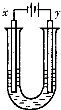
(4)用A元素的单质与B元素的单质可以制成电池,电池中装有KOH浓溶液,用多孔的金属惰性电极浸入KOH溶液,两极均有特制的防止透过的隔膜,在一极通入A的单质,另一极通入B的单质,写出该电池发生的电极反应式:A极________________________;
B极________________________;
(5)若消耗标准状况下A气体11.2L,该电池能提供的电量为________C.
(1)氢 氧 钠 硫 (2)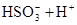

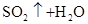
(3)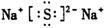 (4)
(4)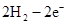


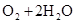
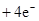


(5)96320
【解析】根据元素的结构及有关性质可知,A,B,C,D分别是H、O、Na、S。
(1)名称分别是氢、氧、钠、硫。
(2)符合条件的两种物质分别是硫酸氢钠和亚硫酸氢钠,方程式为HSO3-+H+=SO2↑+H2O。
(3)钠和S都是活泼的金属和非金属,形成的化学键是离子键,电子式为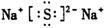 。
。
(4)原电池中负极失去电子,发生氧化反应。正极得到电子,发生还原反应,所以氢气在负极通入,氧气在正极通入。又因为溶液显碱性,所以电极反应式为负极: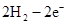

 ,正极:
,正极: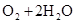
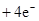

 。
。
(5)氢气是0.5mol,失去1mol电子,所以该电池能提供的电量为6.02×1023×1.6×10-19=96320C。

 名校课堂系列答案
名校课堂系列答案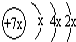 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为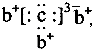 下列比较中正确的是( )
下列比较中正确的是( )| A、原子半径:a>c>d>b | B、最高价含氧酸的酸性c>d>a | C、原子序数:a>d>b>c | D、单质的氧化性a>b>d>c |
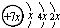 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题: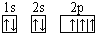

 Al(OH)3+OH-
Al(OH)3+OH-