题目内容
2.某溶液中含有Na+、Mg2+和SO42-三种离子,其中Na+和Mg2+的物质的量分别为0.2mol、0.3mol,则溶液中SO42-的物质的量为( )| A. | 0.4mol | B. | 0.5mol | C. | 0.8mol | D. | 1.6mol |
分析 溶液中阴离子和阳离子所带电荷总量相等,根据电荷守恒来回答.
解答 解:设SO42-物质的量为n,则根据电荷守恒:
0.2mol×1+0.3mol×2=2n,
解得n=0.4mol.
故选A.
点评 本题考查溶液中的电荷守恒知识,可以根据所学知识进行回答,难度不大.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
15.我国新一代气象卫星“风云三号”于今年5月27日成功发射,运载火箭的主要燃料是偏二甲肼(用R表示),其燃烧的化学方程式为:R+2N2O4=3N2+4H2O+2CO2.则R的化学式是( )
| A. | C2H8N2 | B. | N2H4 | C. | CH4 | D. | C6H7N |
15.pH值相等的盐酸(甲)和醋酸(乙),分别与锌反应,若最后锌已全部溶解且放出气体一样多,为此下列说法正确的是( )
| A. | 反应开始时的速率:甲>乙 | |
| B. | 反应结束时,pH值:甲=乙 | |
| C. | 反应开始时,酸的物质的量浓度:甲=乙 | |
| D. | 反应所需时间:甲>乙 |
17.下列说法正确的是( )
| A. | 氧化还原反应一定有氧元素参加 | |
| B. | 氧化还原反应的本质是电子的转移 | |
| C. | 物质中某元素失去电子,则此物质是氧化剂 | |
| D. | 某一反应中有元素化合价的变化,则该反应不一定是氧化还原反应 |
7.设阿伏加德常数为NA.则下列说法正确的是( )
| A. | 28g CO中含有的分子数为NA | |
| B. | 标准状况下,22.4 L H2O所含的分子数为NA | |
| C. | 标准状况下,22.4L H2的质量为1 g | |
| D. | 1mol/L MgCl2溶液中含Mg2+数为NA |
11.生活中的下列物质与水混合,不能形成溶液的是( )
| A. | 食盐 | B. | 白醋 | C. | 白糖 | D. | 面粉 |
10.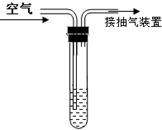 二氧化硫是大气污染物之一.我国的空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如下表所示:
二氧化硫是大气污染物之一.我国的空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如下表所示:
为测定空气中二氧化硫的含量,某中学环保小组的同学利用SO2+I2+2H2O=H2SO4+2HI,设计了如图所示装置进行实验.
(1)将含碘(I2)1.27mg的碘溶液加入到试管中;
(2)向试管内滴加2~3滴淀粉溶液,溶液显蓝色(淀粉遇I2便蓝)
(3)通过抽气装置抽气,使空气由导气管进入试管与碘溶液接触.
(4)当溶液由蓝色变为无色时,测定通过空气的总量为1m3请你通过计算判断,该地区空气中二氧化硫的浓度级别.
 二氧化硫是大气污染物之一.我国的空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如下表所示:
二氧化硫是大气污染物之一.我国的空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如下表所示:| 级别 | 一级指标 | 二级指标 | 三级指标 |
| 浓度限值(mg/m3) | 0.15 | 0.50 | 0.70 |
(1)将含碘(I2)1.27mg的碘溶液加入到试管中;
(2)向试管内滴加2~3滴淀粉溶液,溶液显蓝色(淀粉遇I2便蓝)
(3)通过抽气装置抽气,使空气由导气管进入试管与碘溶液接触.
(4)当溶液由蓝色变为无色时,测定通过空气的总量为1m3请你通过计算判断,该地区空气中二氧化硫的浓度级别.
 .
. .
.