题目内容
向一定量的Fe、FeO和Fe2O3的混合物中加入120mL 4mol/L的稀硝酸,恰好使混合物完全溶解,放出1.344LNO(标准状况),往所得溶液中加入KSCN溶液,无红色出现.若用足量的CO在加热下还原相同质量的混合物,最终得到铁的物质的量为
| A.0.24mol | B.0.21mol | C.0.25mol | D.0.12mol |
B
解析试题分析:n(HNO3)=0.12L×4mol/L=0.48mol,n(NO)=1.344L÷22.4L/mol=0.06mol,往所得溶液中加入KSCN溶液,无红色出现,说明全部生成Fe2+,溶液溶质为Fe(NO3)2,则原混合物中Fe为(0.48mol-0.06mol)÷2==0.21mol,则若用足量的CO在加热下还原相同质量的混合物,最终得到铁的物质的量为0.21mol,故选B。
考点:考查混合物的计算。

溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32?、SO42?、NO3?中的几种。①加入铝片,产生无色无味的气体;②加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如下图所示。则下列说法正确的是( )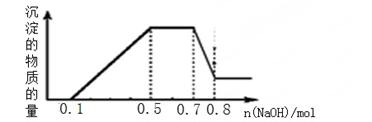
| A.溶液中一定不含CO32?,可能含有SO42?和NO3? |
| B.在滴加NaOH溶液物质的量为0.5至0.7mol时,发生的离子反应为:Al3++4OH-=[Al(OH)4]- |
| C.溶液中的阳离子只有H+、Mg2+、Al3+ |
| D.n(H+)∶n(NH4+)∶n(Mg2+) =2∶4∶1 |
已知在酸性条件下能发生下列反应:Cu+→ Cu+Cu2+(未配平)。NH4CuSO3与足量的2mol·L-1硫酸溶液混合微热,产生下列现象:①有紫红色金属生成;②有刺激性气味气体产生;③溶液呈蓝色。据此判断下列说法一定合理的是
| A.该反应显示硫酸具有酸性 | B.NH4CuSO3中硫元素被氧化 |
| C.刺激性气味的气体是二氧化硫 | D.反应中硫酸作氧化剂 |
碳酸钠(Na2CO3)俗称纯碱,是一种重要的基础化工原料,广泛应用于玻璃、造纸等工业。下列与碳酸钠有关的说法正确的是( )
| A.Na2CO3的稳定性介于Na2CO3·10H2O和NaHCO3之间 |
| B.“侯氏制碱法”制得的碱是指NaHCO3 |
| C.可用盐酸鉴别Na2CO3和NaHCO3固体 |
| D.纯碱有时可代替烧碱使用,比如溶解石英、吸收氯气等 |
物质a、b、c、d均为中学化学中的常见单质或化合物,它们之间的转化关系如右图所示(部分产物已略去),下列各组物质中,通过一步反应就能实现图示转化的是
| 选项 | a | b | c | d |
| A | SO2 | SO3 | S | H2SO4 |
| B | Na2O | Na2O2 | Na | NaOH |
| C | CO | CO2 | C | H2CO3 |
| D | Al2O3 | NaAlO2 | Al | Al(OH)3 |
将0.1mol镁铝合金(Mg17Al12)完全溶解于1.2 L 6mol/L的盐酸中,为使反应后溶液中的Mg2+、Al3+完全沉淀,需加入10 mol/L的氨水至少
| A.0.56L | B.0.70 L | C.0.72L | D.0.84 L |
下列物质的转化在给定条件下不能实现的是
A.Ca(ClO)2(aq)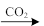 HClO(aq) HClO(aq) HCl(aq) HCl(aq) |
B.H2SiO3 SiO2 SiO2 SiCl4 SiCl4 |
C.Al2O3 NaAlO2(aq) NaAlO2(aq)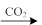 Al(OH)3 Al(OH)3 |
D.Fe2O3 Fe2(SO4)3(aq) Fe2(SO4)3(aq) 无水Fe2(SO4)3 无水Fe2(SO4)3 |
下列解释实验事实的化学方程式正确的是
| A.5molFe和4molCl2反应:5Cl2+4Fe点燃2FeCl2+2FeCl3 |
| B.2molKMnO4和3molH2O2在酸性条件下反应:2MnO4-+3H2O2+6H+=Mn2++4O2↑+6H2O |
| C.在电解液为氢氧化钾的甲醇燃料电池内电路中,阳极的电极反应式为:CH3OH-6e-+8OH-=CO32-+6H2O |
| D.向NaAlO2溶液中通入过量CO2:CO2+3H2O+2AlO2-=2Al(OH)3↓+CO32- |