题目内容
15.下列有机物:①CH3OH ②CH3CH2OH ③CH3CHOHCH2CH3 ④(CH3)2CHCH2OH⑤HOCH2CH(CH3)2⑥(CH3)3COH下列判断正确的是( )| A. | ①②③④⑤⑥之间的关系为同系物 | B. | ③⑥不是同分异构体 | ||
| C. | 可发生消去反应的有机物有4 | D. | 能被催化氧化为醛的有机物有4种 |
分析 ①CH3OH ②CH3CH2OH ③CH3CHOHCH2CH3 ④(CH3)2CHCH2OH⑤HOCH2CH(CH3)2均属于饱和一元醇,且③与④和⑤属于同分异构体,④和⑤为同种物质,⑥(CH3)3COH下含有醛基,属于醛类,据此解答即可.
解答 解:A、依据分析可知:⑥为醛类,与前五种不是同系物,故A错误;
B、③CH3CHOHCH2CH3 分子式为C4H10O,⑥(CH3)3COH分子式为C4H10O,故两者分子式相同,结构不同,属于同分异构体,故B错误;
C、与羟基相连的碳的邻位上含有H原子就能发生消去反应,能发生消去反应的有②CH3CH2OH ③CH3CHOHCH2CH3 ④(CH3)2CHCH2OH⑤HOCH2CH(CH3)2⑥(CH3)3COH,故总共5种,故C错误;
D、端基醇均能被氧化为醛,即:①CH3OH ②CH3CH2OH ④(CH3)2CHCH2OH⑤HOCH2CH(CH3)2能被氧化为醛,故D正确,故选D.
点评 本题主要考查的是同系物、同分异构体的概念,还考查的是醇的性质,醇能发生消去反应和氧化反应,依据反应原理分析即可.

练习册系列答案
 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
4.X、Y、Z、W为周期表中前20号元素中的四种,原子序数依次增大,W、Y为金属元素,X原子的最外层电子数是次外层电子数的3倍,Y、Z位于同周期,Z单质是一种良好的半导体.W能与冷水剧烈反应,Y、Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等.下列说法正确的是( )
| A. | 原子半径:W>Y>Z>X | |
| B. | 气态氢化物的稳定性:X<Z | |
| C. | 最高价氧化物对应水化物的碱性:Y<W | |
| D. | Y、Z的氧化物都有酸性和碱性 |
3.物质的量相同的下列各组有机物,充分燃烧耗氧量相同的一组是( )
| A. | C2H4 C2H6 | B. | C2H4 C3H6 | C. | C2H4 C2H6O | D. | C2H6O C2H4O2 |
10.科学家预测原子序数为114的元素具有相当稳定的核素,它在元素周期表中的位置在第7周期ⅣA族,位于铅的下方,称为类铅.下列关于它的性质叙述中,错误的是( )
| A. | 它的最高价氧化物的水化物是强酸 | B. | 它的金属性比铅强 | ||
| C. | 它具有7个电子层 | D. | 它的最外层电子数为4 |
20.下列物质中不能发生消去反应的是( )
| A. | 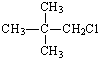 | B. | 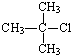 | C. | 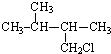 | D. | 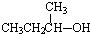 |
7.化学工艺中倡导无污染的绿色化学是一场新的技术革命.若使用单质铜制硝酸铜,下列方案中,耗用原料最经济,而且对环境几乎没有污染的是( )
| A. | Cu和稀硝酸反应制Cu(NO3)2 | |
| B. | Cu和浓硝酸反应制Cu(NO3)2 | |
| C. | 铜在空气中受热转化为CuO,再溶于稀硝酸制Cu(NO3)2 | |
| D. | 铜在氧气中受热转化为CuO,再溶于浓硝酸制Cu(NO3)2 |
4.有5种单核粒子,它们分别是 ${\;}_{19}^{40}$□、${\;}_{18}^{40}$□+、${\;}_{19}^{40}$□+、${\;}_{20}^{40}$□2+、${\;}_{20}^{41}$□(“□”内元素符号未写出),则它们所属元素的种类有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
5.某化合物的性质如下:①加入氢氧化钠溶液,加热,产生使湿润的红色石蕊试纸变蓝的气体;②溶于水,加入硝酸钡溶液,产生能溶于稀硝酸的白色沉淀.则该物质是( )
| A. | NH4Cl | B. | (NH4)2CO3 | C. | NaCl | D. | K2SO4 |
 如图所示的原电池装置,则:
如图所示的原电池装置,则: