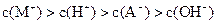题目内容
(15分)有一白色固体混合物,可能含有有的阴、阳离子分别是
为了鉴定其中的离子,现进行如下实验,根据实验现象,填写下列表格:
(1)取该粉末,加水后得到无色溶液,且未嗅到气味;用pH试纸测得溶液的pH为12。
(2)向溶液中滴加盐酸溶液,开始有沉淀生成,继续滴加,沉淀消失,同时有无色无味气体逸出。
(3)尚待检验的离子及其检验方法
| 阳离子 | K+ Ba2+ Ag+ Mg2+ NH4+ Na+ |
| 阴离子 | SO42- SO32- CO32- AlO2- |
(1)取该粉末,加水后得到无色溶液,且未嗅到气味;用pH试纸测得溶液的pH为12。
| 排除的离子 | 排除的依据 |
| | |
| 肯定存在的离子 | 判断依据 |
| | |
| 排除的离子 | 排除的依据 |
| | |
| 尚待检验的离子 | 检验方法 |
| | |
(1)
| 排除的离子 | 排除的依据 |
| NH4+ Ag+、Mg2+ | 由于溶液呈碱性,且未嗅到刺激性气味 碱性溶液中无沉淀生成 |
| 肯定存在的离子 | 判断依据 |
| AlO2- CO32- | 加酸有沉淀,继续加酸沉淀溶解 加酸后有无色无味气体逸出 |
| 排除的离子 | 排除的依据 |
| Ba2+ SO32- | 有CO32-存在时原溶液无沉淀 酸化后逸出的气体没有刺激性气味 |
| 尚待检验的离子 | 检验方法 |
| K+、Na+ SO42- | 焰色反应 酸性溶液中滴加BaCl2溶液,是否有白色沉淀生成 |
(1)因为溶液的pH为12,即溶液呈碱性,且未嗅到刺激性气味,在不存在NH4+,又因为得到的是无色的溶液,说明没有生成沉淀,则不存在Ag+、Mg2+。
(2)因为向溶液中滴加盐酸溶液,开始有沉淀生成,继续滴加,沉淀消失,说明溶液中存在AlO2-;同时有无色无味气体逸出,说明存在CO32-,且没有SO32-,因为有CO32-,则一定没有Ba2+。
(3)经过上述两个实验,还没确定的离子有K+、Na+、SO42-。其中K+、Na+用焰色反应检验,若火焰呈黄色,则说明有Na+,透过蓝色钴玻璃火焰呈紫色,则说明含有K+;稀氨溶液中加入盐酸酸化后加入BaCl2溶液,观察是否有白色沉淀生成,以判断是否含有SO42-。
(2)因为向溶液中滴加盐酸溶液,开始有沉淀生成,继续滴加,沉淀消失,说明溶液中存在AlO2-;同时有无色无味气体逸出,说明存在CO32-,且没有SO32-,因为有CO32-,则一定没有Ba2+。
(3)经过上述两个实验,还没确定的离子有K+、Na+、SO42-。其中K+、Na+用焰色反应检验,若火焰呈黄色,则说明有Na+,透过蓝色钴玻璃火焰呈紫色,则说明含有K+;稀氨溶液中加入盐酸酸化后加入BaCl2溶液,观察是否有白色沉淀生成,以判断是否含有SO42-。

练习册系列答案
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
 c(S2-)+c(HS-)+c(H2S)
c(S2-)+c(HS-)+c(H2S)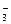 、MnO
、MnO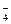
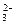 、CO
、CO