题目内容
有关3BrF3+5H2O═HBrO3+Br2+9HF+O2↑反应的叙述,正确的是( )
| A、还原剂与氧化剂的物质的量之为5:3 |
| B、HBrO3和HF是还原产物 |
| C、生成1mol O2,5mol H2O被氧化 |
| D、BrF3既是氧化剂又是还原剂 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:3BrF3+5H2O═HBrO3+Br2+9HF+O2↑中,Br元素的化合价由+3价升高为+5价,O元素的化合价由-2价升高为0,Br元素的化合价由+3价降低为0,以此来解答.
解答:
解:A.由反应可知,2molH2O和1molBrF3作氧化剂,2molBrF3作还原剂,则还原剂与氧化剂的物质的量之为2:3,故A错误;
B.F元素的化合价不变,则只有HBrO3是还原产物,故B错误;
C.生成1mol O2,由O原子守恒可知,2mol H2O被氧化,故C错误;
D.Br元素的化合价既升高又降低,则BrF3既是氧化剂又是还原剂,故D正确;
故选D.
B.F元素的化合价不变,则只有HBrO3是还原产物,故B错误;
C.生成1mol O2,由O原子守恒可知,2mol H2O被氧化,故C错误;
D.Br元素的化合价既升高又降低,则BrF3既是氧化剂又是还原剂,故D正确;
故选D.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,注意元素化合价的判断,题目难度不大.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
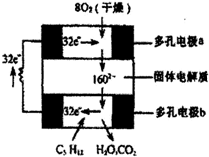 设计出燃料电池使汽油(设其成分为C5H12)氧化直接产生电流,是21世纪最富有挑战性的课题之一.最近有人设计了一种固体燃料电池,以掺杂了氧化钇的固体氧化锆为电解质.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列关于该电池的判断中,错误的是( )
设计出燃料电池使汽油(设其成分为C5H12)氧化直接产生电流,是21世纪最富有挑战性的课题之一.最近有人设计了一种固体燃料电池,以掺杂了氧化钇的固体氧化锆为电解质.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列关于该电池的判断中,错误的是( )| A、该电池的正极反应式为:O2+2H2O+4e-=4OH- |
| B、氧化钇和氧化锆的化学式分别为Y2O3和ZrO2,掺杂氧化钇的氧化锆晶体中存在晶体缺陷,其导电性比纯氧化锆晶体强得多 |
| C、该燃料电池外部的电流方向为正极一负极,内部阴离子向负极移动 |
| D、燃料电池相对于汽油直接燃烧,具有较高的能量利用率 |
下列有关生活常识的说法中,正确的是( )
| A、天然果汁中不含任何化学物质 |
| B、味精的主要成分为蛋白质,烧菜时刻加入适量 |
| C、“绿色食品”是指颜色一定为绿色的食品 |
| D、烧鱼时放点醋,可软化鱼骨 |
某溶液中加入铝粉有氢气产生,该溶液中肯定可以大量共存的离子组是( )
| A、Na+、NO3-、Cl-、CO32- |
| B、Na+、K+、Ba2+、HCO3- |
| C、Fe3+、K+、SO42-、Cl- |
| D、Na+、K+、Cl-、SO42- |
下列说法不正确的是( )
| A、水晶、玛瑙、光导纤维这些物质的主要成分是SiO2 |
| B、SiO2为酸性氧化物,能与强碱反应,但不能与酸反应 |
| C、装NaOH的试剂瓶不能用玻璃塞,因为SiO2与NaOH反应生成的Na2SiO3具有粘性 |
| D、计算机芯片CPU主要成分是单晶硅 |
下列各组离子,在水溶液中能大量共存的是( )
(1)K+ Fe2+ SO42- ClO- (2)K+ Al3+ Cl- CO32-
(3)ClO- Cl- K+ OH-(4)Fe3+ Cu2+ SO42- Cl-
(5)Na+ K+ AlO2- HCO3- (6)H+ Fe2+ SO42- NO3-.
(1)K+ Fe2+ SO42- ClO- (2)K+ Al3+ Cl- CO32-
(3)ClO- Cl- K+ OH-(4)Fe3+ Cu2+ SO42- Cl-
(5)Na+ K+ AlO2- HCO3- (6)H+ Fe2+ SO42- NO3-.
| A、(1)和(6) |
| B、(3)和(4) |
| C、(1)和(4) |
| D、(2)和(5) |
影响一定量气体体积的主要因素是( )
| A、微粒间的平均距离 |
| B、微粒本身的大小 |
| C、微粒的质量 |
| D、气体分子的微粒数 |
下列化学用语书写不正确的是( )
A、甲烷的电子式: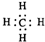 | ||
B、氟化钠的电子式: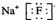 | ||
| C、硫离子的电子式:S2- | ||
D、碳-12原子:
|