题目内容
16.水是生命之源,也是最宝贵的资源之一.下列表述正确的是( )| A. | 水是弱电解质 | B. | 4℃时,纯水的pH=7 | ||
| C. | 可燃冰是可以燃烧的水 | D. | 氢氧两种元素只能组成水 |
分析 A、水存在微弱的电离,属于弱电解质;
B、水的电离是吸热反应,常温下水的pH=7;
C、可燃冰的主要成分是甲烷;
D、氢氧两种元素可以组成双氧水.
解答 解:A、水能微弱电离出氢离子和氢氧根离子,属于弱电解质,故A正确;
B、水的电离是吸热反应,常温下水的pH=7,常温是25℃,故B错误;
C、可燃冰的主要成分是甲烷,不是水,故C错误;
D、氢氧两种元素可以组成水和双氧水,故D错误,
故选A.
点评 本题主要考查的是弱电解质的概念、水的电离以及元素组成物质,难度不大,属于常考题.

练习册系列答案
相关题目
4.能够将溶液和胶体区分开的方法是( )
| A. | 利用丁达尔效应 | B. | 观察颜色、状态 | C. | 过滤 | D. | 闻气味 |
1.下列有关电解质的叙述正确的是( )
| A. | 在熔融状态下能导电的物质一定是电解质 | |
| B. | 弱电解质溶液的导电能力可能比强电解质溶液的导电能力强 | |
| C. | 向0.1mol/L的氨水中加入少量醋酸铵固体,则溶液中c$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$增大 | |
| D. | 两种醋酸溶液的物质的量浓度分别为c1=0.1mol/L和c2=0.01mol/L,c(H+)分别为amol/L和bmol/L则a=10b |
8.磷的单质和化合物有着重要的应用.磷酸铁(FePO4•2H2O,难溶于水的米白色固体)可用于药物、食品添加剂和锂离子电池的正极材料,下列实验可制备磷酸铁.
(1)称取一定量已除去油污的废铁屑,加入稍过量的稀硫酸,加热、搅拌,反应一段时间后过滤,反应加热的目的是加快Fe和稀硫酸的反应速率.
(2)为了使滤液中的Fe2+完全被H2O2氧化,下列实验条件控制正确的是AB(填序号).
A.加入适当过量的H2O2溶液 B.缓慢滴加H2O2溶液并搅拌
C.加热,使反应在较高温度下进行 D.用氨水调节pH=7
(3)将一定量的Na2HPO4溶液(溶液显碱性)加入含有Fe3+的溶液中,搅拌、过滤、洗涤、干燥得到FePO4•2H2O.若反应得到的FePO4•2H2O固体呈棕黄色,则磷酸铁中混有的杂质可能为Fe(OH)3(写化学式).
(4)化学反应的能量变化(△H)与反应物和生成物的键能有关.键能可简单的理解为断开1 mol 化学键时所吸收的能量.下表是部分化学键的键能数据:
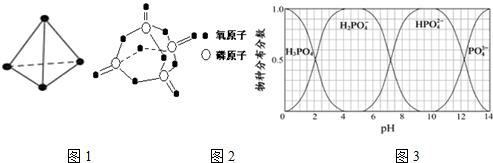
已知白磷固体(P4 结构如图1所示)的燃烧热为.2378.0kJ/mol,白磷完全燃烧的固体产物结构如图2所示,则白磷燃烧的热化学方程式为P4(s)+5O2(g)=P4O10(s)△H=-2378.0kJ/mol;上表中X=434.
(5)NaH2PO4、Na2HPO4和Na3PO4可通过H3PO4与NaOH溶液反应获得,含磷各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如图3所示.为获得尽可能纯的NaH2PO4,pH应控制在4~5.5(介于此区间内的任意值或区间均可);pH=8时,溶液中主要含磷物种浓度大小关系为c(HPO42-)>c(H2PO4-).

(1)称取一定量已除去油污的废铁屑,加入稍过量的稀硫酸,加热、搅拌,反应一段时间后过滤,反应加热的目的是加快Fe和稀硫酸的反应速率.
(2)为了使滤液中的Fe2+完全被H2O2氧化,下列实验条件控制正确的是AB(填序号).
A.加入适当过量的H2O2溶液 B.缓慢滴加H2O2溶液并搅拌
C.加热,使反应在较高温度下进行 D.用氨水调节pH=7
(3)将一定量的Na2HPO4溶液(溶液显碱性)加入含有Fe3+的溶液中,搅拌、过滤、洗涤、干燥得到FePO4•2H2O.若反应得到的FePO4•2H2O固体呈棕黄色,则磷酸铁中混有的杂质可能为Fe(OH)3(写化学式).
(4)化学反应的能量变化(△H)与反应物和生成物的键能有关.键能可简单的理解为断开1 mol 化学键时所吸收的能量.下表是部分化学键的键能数据:
| 化学键 | P-P | P-O | O=O | P=O |
| 键能/kJ•mol-1 | 197 | 360 | 499 | X |
(5)NaH2PO4、Na2HPO4和Na3PO4可通过H3PO4与NaOH溶液反应获得,含磷各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如图3所示.为获得尽可能纯的NaH2PO4,pH应控制在4~5.5(介于此区间内的任意值或区间均可);pH=8时,溶液中主要含磷物种浓度大小关系为c(HPO42-)>c(H2PO4-).
5.1000mL某待测液中除含有0.2mol•L-1的Na+外,还可能含有下列离子中的一种或多种:
现进行如下实验操作(所加试剂均过量):

(1)写出生成白色沉淀B的离子方程式:HCO3-+Ba2++OH-=BaCO3↓+H2O.
(2)待测液中肯定不存在的阳离子是Fe3+、Ba2+.
(3)若无色气体D是混合气体:
①待测液中一定含有的阴离子是CO32-、HCO3-、SO32-.
②沉淀A中能还原稀硝酸的成分是BaSO3(写化学式).
| 阳离子 | K+、NH4+、Fe3+、Ba2+ |
| 阴离子 | Cl-、Br-、CO32-、HCO3-、SO32-、SO42- |

(1)写出生成白色沉淀B的离子方程式:HCO3-+Ba2++OH-=BaCO3↓+H2O.
(2)待测液中肯定不存在的阳离子是Fe3+、Ba2+.
(3)若无色气体D是混合气体:
①待测液中一定含有的阴离子是CO32-、HCO3-、SO32-.
②沉淀A中能还原稀硝酸的成分是BaSO3(写化学式).
 .
.