题目内容
安徽省从2013年12月1日零时起,车用汽油升级为“国Ⅳ”标准,对二氧化硫的排放有了大大的改善。已知SO2可以用Fe( NO3)3溶液吸收, 0.1mol/L的Fe(NO3)3溶液的pH=2。某学习小组据此展开如下相关探究:
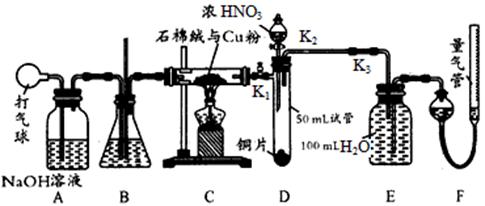
【探究I】铜与浓硫酸的反应探究:
(l)取12.8g铜片于三颈烧瓶中,通N2一段时间后再加入20 mL 18 mol?L-1的浓硫酸,加热。装置A中有白雾(硫酸酸雾)生成,装置B中产生白色沉淀,充分反应后,烧瓶中仍有铜片剩余。
①该小组同学认为烧瓶中除有铜片剩余外还应有较多的硫酸剩余,其原因是: ___________________ 。
②该小组同学欲通过测定产生气体的量来求余酸的物质的量,设计了多种实验方案。下列方案不可行的是______ 。
A.将产生的气体缓缓通过预先称量的盛有碱石灰的干燥管,结束反应后再次称重
B.将产生的气体缓缓通入足量硫酸酸化的高锰酸钾溶液后,再加入足量的BaCl2溶液,测量所得沉淀的质量
C.用排饱和NaHSO3溶液的方法测定其产生气体的体积(折算成标准状况)
【探究II】装置B中产生沉淀的原因探究:
(2)加入浓硫酸之前先通N2一段时间,其目的是____ 。
(3)经过讨论,该小组对装置B中产生沉淀的原因,提出下列猜想(不考虑各因素的叠加):
猜想1: 装置A中的白雾进入B参与反应
猜想2:SO2被Fe3+氧化为SO42-
猜想3: 。
(4)甲同学认为只要在装置A、B间增加洗气瓶C,就可以排除装置A中白雾影响,则C中盛放的试剂是 。
(5)乙同学取出少量装置B中清液,加入几滴酸性高锰酸钾,发现紫红色褪去,据此认为猜想2成立。你是否同意其结论?并说明理由: 。
【思考与交流】
(6)实验结束后,若使烧瓶中铜片继续溶解,下列方案(必要时可加热)可行的是 。
A.打开弹簧夹,通入O2 B.由分液漏斗加入H2O2溶液
C.由分液漏斗加入NaNO3溶液 D.由分液漏斗加入Na2SO4溶液
(1)①随着反应进行,硫酸变稀,与铜片不反应 ②A B
(2)排除空气的干扰
(3)酸性条件下,SO2被NO3-氧化为SO42-
(4)NaHSO3饱和溶液
(5)不同意;溶解的SO2也能使酸性高锰酸钾溶液褪色
(6)A B C
解析试题分析:(1)①Cu只与浓硫酸发生反应。随着反应的进行硫酸变为稀硫酸,就与铜片不反应。所以烧瓶中除有铜片剩余外还应有较多的硫酸剩余。②A.发生在加热条件下进行。所以产生的气体除了有SO2外,还有水蒸汽,因此缓缓通过预先称量的盛有碱石灰的干燥管,结束反应后再次称重称量的质量是SO2和水蒸汽的质量和。无法计算剩余硫酸的质量。错误。B.高锰酸钾能把SO2氧化为硫酸,由于是用硫酸酸化,所以再加入足量的BaCl2溶液,测量所得沉淀是SO2氧化的硫酸和加入的硫酸共同产生的硫酸钡。故不能确定SO2的多少,进而不能确定有多少硫酸没有乘积反应。错误。C.由于SO2不能在饱和NaHSO3溶液中溶解。所以可以用排饱和NaHSO3溶液的方法测定其产生气体的体积(折算成标准状况)。来确定发生还原反应的硫酸的物质的量,进而可以计算出未参加反应的硫酸的物质的量。正确。选项为AB。(2)加入浓硫酸之前先通N2一段时间,其目的是驱赶装置中的空气,排除空气的干扰。(3)根据题意可知:猜想3是酸性条件下,SO2被NO3-氧化为SO42-。(4)甲同学认为只要在装置A、B间增加洗气瓶C,就可以排除装置A中白雾影响,则C中盛放的试剂应该只吸收SO3但是不溶解或反应消耗SO2,可以是NaHSO3饱和溶液。(5)乙同学取出少量装置B中清液,加入几滴酸性高锰酸钾,发现紫红色褪去,据此认为猜想2成立这种认识是错误的、不同意;因为溶解的SO2也能使酸性高锰酸钾溶液褪色。 (6)A 通入氧气,发生反应:2Cu+ O2 2CuO;CuO + H2SO4= CuSO4 + H2O.正确。B由分液漏斗加入H2O2溶液H2O2加热分解产生氧气,作用同A。正确。C由分液漏斗加入NaNO3溶液。在酸性条件下发生反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O。Cu溶解。正确。D.由分液漏斗加入Na2SO4溶液不会发生任何反应。错误。因此选项为A B C。
2CuO;CuO + H2SO4= CuSO4 + H2O.正确。B由分液漏斗加入H2O2溶液H2O2加热分解产生氧气,作用同A。正确。C由分液漏斗加入NaNO3溶液。在酸性条件下发生反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O。Cu溶解。正确。D.由分液漏斗加入Na2SO4溶液不会发生任何反应。错误。因此选项为A B C。
考点:考查铜与浓硫酸的反应的探究及产物SO2的性质及检验的知识。

 开心快乐假期作业暑假作业西安出版社系列答案
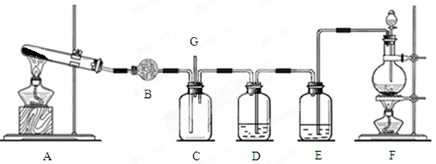
开心快乐假期作业暑假作业西安出版社系列答案为了探究AgNO3的热稳定性,某化学兴趣小组设计了如下实验。用如图所示的实验装置A加热AgNO3固体,产生红棕色气体,在装置D中收集到无色气体。当反应结束后,试管中残留固体为黑色。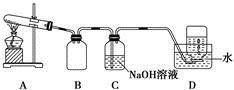
(1)装置B的作用是 。
(2)经小组讨论并验证该无色气体为O2,其验证方法是 。
(3)【查阅资料】Ag2O和粉末状的Ag均为黑色;Ag2O可溶于氨水。
【提出设想】试管中残留的黑色固体可能是:ⅰ.Ag;ⅱ.Ag2O;ⅲ.Ag和Ag2O。
【实验验证】该小组为验证上述设想,分别取少量黑色固体放入试管中,进行了如下实验。
| 实验编号 | 操作 | 现象 |
| a | 加入足量氨水,振荡 | 黑色固体不溶解 |
| b | 加入足量稀硝酸,振荡 | 黑色固体溶解,并有气体产生 |
【实验评价】根据上述实验,不能确定固体产物成分的实验是 (填实验编号)。
【实验结论】根据上述实验结果,该小组得出AgNO3固体热分解的产物有 。
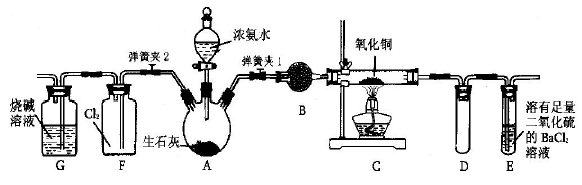
下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。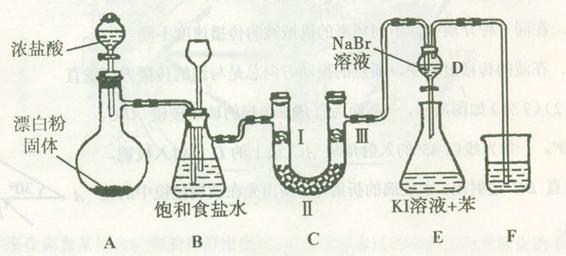
(1)装置A是氯气的发生装置,请写出相应反应的化学方程式: 。
(2)装置B中饱和食盐水的作用是 ;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象: 。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III处依次放入物质的组合应是 (填字母编号)。
| 编号 | I | II | III |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(4)设计装置D、E的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是 ,该现象 (填“能”或“不能”)说明溴单质的氧化性强于碘,原因是 。
(5)装置F的作用是 ,其烧杯中的溶液不能选用下列中的 (填字母编号)。
a.饱和NaOH溶液 b.饱和Ca(OH)2溶液
c.饱和Na2SO3溶液 d.饱和Na2CO3溶液