题目内容
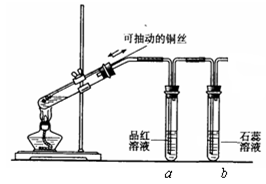
(16分)几位同学设计实验观察铜与浓硫酸的反应,检验生成的气体的性质。甲设计了如图所示的装置,在大试管里加入2mL浓硫酸,用带导管和一个小孔的胶管塞紧,从孔中插入一根铜丝,加热,把产生的气体依次通入品红溶液和石蕊溶液中。
请回答下列问题:
(1)写出铜与浓硫酸反应的化学方程式: 。
(2)试管b中的现象是 ,
通过试管a、b的现象得出的结论是 。
(3)乙同学认为甲同学的设计不能全面体现SO2的性质,他打算增加试管进行其它实验。以下为增加的试管中盛放的试剂:A. 澄清石灰水 B. KMnO4(aq) C. 氢硫酸
请你帮助乙同学作出选择,在横线上先写出字母,再用文字简单说明实验的目的。
(4)丙同学评价甲同学的实验装置既有优点也有不足,优点是
,不足之处改进的具体措施是 。
(5)若把上述装置中大试管的浓硫酸换成稀硝酸,试管a和b作如下改变(其中a装满水,b空置),则在大试管中发生的反应的离子方程式为 ,
试管a的作用是 。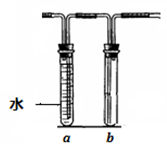
请回答下列问题:

(1)写出铜与浓硫酸反应的化学方程式: 。
(2)试管b中的现象是 ,
通过试管a、b的现象得出的结论是 。
(3)乙同学认为甲同学的设计不能全面体现SO2的性质,他打算增加试管进行其它实验。以下为增加的试管中盛放的试剂:A. 澄清石灰水 B. KMnO4(aq) C. 氢硫酸
请你帮助乙同学作出选择,在横线上先写出字母,再用文字简单说明实验的目的。
(4)丙同学评价甲同学的实验装置既有优点也有不足,优点是
,不足之处改进的具体措施是 。
(5)若把上述装置中大试管的浓硫酸换成稀硝酸,试管a和b作如下改变(其中a装满水,b空置),则在大试管中发生的反应的离子方程式为 ,
试管a的作用是 。

(1)Cu + 2H2SO4(浓)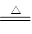 CuSO4 + SO2↑+ 2H2O (2分)
CuSO4 + SO2↑+ 2H2O (2分)
(2)紫色溶液变红色(1分),SO2是一种酸性气体,具有漂白性(能漂白品红)(2分)
(3)B,验证SO2的还原性;C,验证SO2的氧化性。(各1分)
(4)使用可抽动的铜丝能随时控制反应的开始和结束,节约药品用量,减少污染气体的产生(2分); 把尾气通入NaOH溶液中(1分)。
(5)3Cu2+ + 8H+ + 2NO3- = 3Cu2+ + 2NO↑+ 4H2O (2分);
除去NO2,排水法收集纯净的NO(2分)。
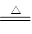 CuSO4 + SO2↑+ 2H2O (2分)
CuSO4 + SO2↑+ 2H2O (2分)(2)紫色溶液变红色(1分),SO2是一种酸性气体,具有漂白性(能漂白品红)(2分)
(3)B,验证SO2的还原性;C,验证SO2的氧化性。(各1分)
(4)使用可抽动的铜丝能随时控制反应的开始和结束,节约药品用量,减少污染气体的产生(2分); 把尾气通入NaOH溶液中(1分)。
(5)3Cu2+ + 8H+ + 2NO3- = 3Cu2+ + 2NO↑+ 4H2O (2分);
除去NO2,排水法收集纯净的NO(2分)。
(1)浓硫酸具有强氧化性,在加热的条件下能氧化铜生成硫酸铜。
(2)浓硫酸的还原产物是SO2,SO2溶于水显酸性,所以紫色溶液变红色。SO2能使品红溶液褪色,具有漂白性。
(3)SO2中S的化合价是+4价,处于中间价态,既有氧化性,又有还原性。因此可以通过酸性高锰酸钾溶液来验证其还原性。通过硫化氢来验证其氧化性。
(4)根据装置的特点可判断,通过使用可抽动的铜丝能随时控制反应的开始和结束,节约药品用量,减少污染气体的产生。但由于SO2属于大气污染为,反应结束后需要进行尾气处理,可将尾气通入氢氧化钠溶液中。
(5)硝酸具有强氧化性,也能把铜氧化生成硝酸铜,而硝酸被还原生成NO2或NO气体。NO不溶于水,NO2溶于水生成NO,所以可利用排水法收集纯净的NO。
(2)浓硫酸的还原产物是SO2,SO2溶于水显酸性,所以紫色溶液变红色。SO2能使品红溶液褪色,具有漂白性。
(3)SO2中S的化合价是+4价,处于中间价态,既有氧化性,又有还原性。因此可以通过酸性高锰酸钾溶液来验证其还原性。通过硫化氢来验证其氧化性。
(4)根据装置的特点可判断,通过使用可抽动的铜丝能随时控制反应的开始和结束,节约药品用量,减少污染气体的产生。但由于SO2属于大气污染为,反应结束后需要进行尾气处理,可将尾气通入氢氧化钠溶液中。
(5)硝酸具有强氧化性,也能把铜氧化生成硝酸铜,而硝酸被还原生成NO2或NO气体。NO不溶于水,NO2溶于水生成NO,所以可利用排水法收集纯净的NO。

练习册系列答案
相关题目