题目内容
一定温度下,难溶电解质在饱和溶液中各离子浓度幂的乘积是一个常数,这个常数称为该难溶电解质的溶度积,用符号Ksp表示。
即:AmBn(s) mAn+(aq)+nBm-(aq) [An+]m·[Bm-]n=Ksp
mAn+(aq)+nBm-(aq) [An+]m·[Bm-]n=Ksp
已知:某温度时,Ksp(AgCl)=[Ag+][Cl-] =1.8×10-10
Ksp(Ag2CrO4)=[Ag+]2[CrO2- 4] =1.1×10-12
1.81/2="1.3 " 2751/3=6.5
试求:
(1)此温度下AgCl饱和溶液和Ag2CrO4饱和溶液的物质的量浓度,并比较两者的大小。
(2)此温度下,在0.010mo1·L-1的AgNO3溶液中,AgCl与Ag2CrO4分别能达到的最大物质的量浓度,并比较两者的大小。
即:AmBn(s)
 mAn+(aq)+nBm-(aq) [An+]m·[Bm-]n=Ksp
mAn+(aq)+nBm-(aq) [An+]m·[Bm-]n=Ksp已知:某温度时,Ksp(AgCl)=[Ag+][Cl-] =1.8×10-10
Ksp(Ag2CrO4)=[Ag+]2[CrO2- 4] =1.1×10-12
1.81/2="1.3 " 2751/3=6.5
试求:
(1)此温度下AgCl饱和溶液和Ag2CrO4饱和溶液的物质的量浓度,并比较两者的大小。
(2)此温度下,在0.010mo1·L-1的AgNO3溶液中,AgCl与Ag2CrO4分别能达到的最大物质的量浓度,并比较两者的大小。
①AgCl(s) Ag+(a
Ag+(a q)+Cl-(aq)
q)+Cl-(aq)
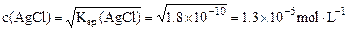 (1分)
(1分)
Ag2CrO4(s) 2Ag+(aq)+CrO42-(aq)
2Ag+(aq)+CrO42-(aq)
2x x
(2x)2·x=Ksp
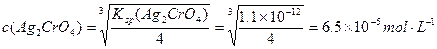 (1分)
(1分)
∴ c(AgCl)<c(Ag2CrO4) (1分)
②在0.010 mol·L-1 AgNO3溶液中,c(Ag+)="0.010" mol·L-1
AgCl(s) Ag+(aq) + Cl-(aq)
Ag+(aq) + Cl-(aq)
溶解平衡时: 0.0 10+x x
10+x x
(0.010+x)·x=1.8×10-10 ∵ x很小,∴ 0.010+x ≈0.010
x=1.8×10-8(mol·L-1)
c(AgCl)= 1.8×10-8(mol·L-1) (1分)
Ag2CrO4(s) 2Ag+(aq) + CrO2-4(aq)
2Ag+(aq) + CrO2-4(aq)
溶解平衡时: 0.010+x x
(0.010+2x)2·x=1.1×10-12
∵ x很小,∴ 0.010+2x≈0.010
x=1.1×10-8(mol·L-1)
∴ c(Ag2CrO4)=1.1×10-8 (mol·L-1) (1分)
∴ c(AgCl)>c(Ag2CrO4) (1分)
 Ag+(a
Ag+(a q)+Cl-(aq)
q)+Cl-(aq)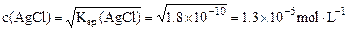 (1分)
(1分)Ag2CrO4(s)
 2Ag+(aq)+CrO42-(aq)
2Ag+(aq)+CrO42-(aq)2x x
(2x)2·x=Ksp
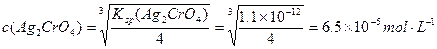 (1分)
(1分)∴ c(AgCl)<c(Ag2CrO4) (1分)
②在0.010 mol·L-1 AgNO3溶液中,c(Ag+)="0.010" mol·L-1
AgCl(s)
 Ag+(aq) + Cl-(aq)
Ag+(aq) + Cl-(aq)溶解平衡时: 0.0
 10+x x
10+x x(0.010+x)·x=1.8×10-10 ∵ x很小,∴ 0.010+x ≈0.010
x=1.8×10-8(mol·L-1)
c(AgCl)= 1.8×10-8(mol·L-1) (1分)
Ag2CrO4(s)
 2Ag+(aq) + CrO2-4(aq)
2Ag+(aq) + CrO2-4(aq)溶解平衡时: 0.010+x x
(0.010+2x)2·x=1.1×10-12
∵ x很小,∴ 0.010+2x≈0.010
x=1.1×10-8(mol·L-1)
∴ c(Ag2CrO4)=1.1×10-8 (mol·L-1) (1分)
∴ c(AgCl)>c(Ag2CrO4) (1分)
略

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
 Mg2++ 2OH―,加入下列哪种固体物质可使Mg(OH)2固体的质量减少
Mg2++ 2OH―,加入下列哪种固体物质可使Mg(OH)2固体的质量减少

 5Ca2++3 PO43-+OH-。已知Ca5(PO4)3F(s)的溶解度比a5(PO4)3OH(s)更小,为了保护牙齿,世界各地均采用了不同的措施。以下措施中不能保护牙齿的是( )
5Ca2++3 PO43-+OH-。已知Ca5(PO4)3F(s)的溶解度比a5(PO4)3OH(s)更小,为了保护牙齿,世界各地均采用了不同的措施。以下措施中不能保护牙齿的是( ) 的溶度积常数Ksp=c(Ag+)×c(Cl-)=1×10-10。(混合后溶液的体积变化忽略不计)。试计算:
的溶度积常数Ksp=c(Ag+)×c(Cl-)=1×10-10。(混合后溶液的体积变化忽略不计)。试计算: