��Ŀ����
����Ŀ��A��B��C��W��Ϊ��ѧ�����Ĵ��������֮��������ת����ϵ���������P��Ӧ��������ȥ����Ӧ������ˮ��Һ�н��У���
![]()
��1����A��B��C�������ʵ���Һ���Լ��ԣ���ɫ��Ӧ��Ϊ��ɫ�����ȷֽ��ת��ΪB��
��A�����Wת��ΪC���ܷ�Ӧ�����ӷ���ʽΪ__��
��A��Һ��C��Һ��Ӧ�Ļ�ѧ����ʽΪ__��
��2����B����Һ�Ի�ɫ��һ��������B�ı�����Һ�����ˮ��Ӧ���ɺ��ɫ��ɢϵ��
��ʵ������A���ʵķ�Ӧ�����ӷ���ʽΪ__��
��C��Һ�м�������������Һ������__��
��һ��������W��ˮ��Ӧ�Ļ�ѧ����ʽΪ___��
���𰸡�OH-+CO2=HCO3- NaOH+NaHCO3=Na2CO3+H2O MnO2+4H++2Cl-![]() Mn2++2H2O+Cl2�� ���ɰ�ɫ��������ת��Ϊ����ɫ�����ձ�Ϊ���ɫ 3Fe+4H2O(g)
Mn2++2H2O+Cl2�� ���ɰ�ɫ��������ת��Ϊ����ɫ�����ձ�Ϊ���ɫ 3Fe+4H2O(g)![]() Fe3O4+4H2
Fe3O4+4H2
��������
(1)��A��B��C�������ʵ���Һ���Լ��ԣ���ɫ��Ӧ��Ϊ��ɫ��C���ȷֽ��ת��ΪB������NaԪ�أ�CΪNaHCO3��BΪNa2CO3�����ͼ��ת����֪��AΪNaOH��WΪCO2��
��2����B����Һ�Ի�ɫ��һ��������B�ı�����Һ�����ˮ��Ӧ���ɺ��ɫ��ɢϵ��BΪFeCl3�����ͼ��ת����֪��AΪCl2��WΪFe��CΪFeCl2��
(1)��A��B��C�������ʵ���Һ���Լ��ԣ���ɫ��Ӧ��Ϊ��ɫ��C���ȷֽ��ת��ΪB������NaԪ�أ�CΪNaHCO3��BΪNa2CO3�����ͼ��ת����֪��AΪNaOH��WΪCO2��
��A�����Wת��ΪC���ܷ�Ӧ�����ӷ���ʽΪOH-+CO2=HCO3-
��A��Һ��C��Һ��Ӧ�Ļ�ѧ����ʽΪ NaOH+NaHCO3=Na2CO3+H2O
��2����B����Һ�Ի�ɫ��һ��������B�ı�����Һ�����ˮ��Ӧ���ɺ��ɫ��ɢϵ��BΪFeCl3�����ͼ��ת����֪��AΪCl2��WΪFe��CΪFeCl2��
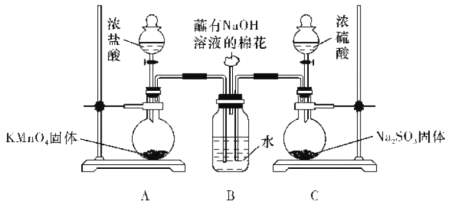
��ʵ������A���ʵķ�Ӧ�����ӷ���ʽΪMnO2+4H++2Cl-![]() Mn2++2H2O+Cl2��
Mn2++2H2O+Cl2��
��C��Һ�м�������������Һ���������ɰ�ɫ��������ת��Ϊ����ɫ�����ձ�Ϊ���ɫ
��һ��������W��ˮ��Ӧ�Ļ�ѧ����ʽΪ3Fe+4H2O(g)![]() Fe3O4+4H2
Fe3O4+4H2

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ���¶�ΪT ʱ����2.0 L�����ܱ������г���1.0 mol PCl5��
��Ӧ��PCl5(g)![]() PCl3(g)��Cl2(g)��һ��ʱ���ﵽƽ�⣬��Ӧ�����вⶨ�IJ������ݼ��±���
PCl3(g)��Cl2(g)��һ��ʱ���ﵽƽ�⣬��Ӧ�����вⶨ�IJ������ݼ��±���
t/s | 0 | 50 | 150 | 250 | 250 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
����˵����ȷ����
A. ��Ӧ��ǰ50 s�ڵ�ƽ������v(PCl3)=0.0032mol/(L��s)
B. ���������������䣬�����¶ȣ�ƽ��ʱc(PCl3)=0.11mol/L���÷�ӦΪ���ȷ�Ӧ
C. ��ͬ�¶��£���ʼʱ�������г���1.0 mol PCl5��0.20 mol PCl3��0.20 mol Cl2���ﵽƽ��ǰ��v����v��
D. ��ͬ�¶��£���ʼʱ�������г���2.0 mol PCl3��2.0 mol Cl2���ﵽƽ��ʱ��PCl3��ת����С��80��
����Ŀ��I��300��ʱ��������X������Y��0.16mol����10L�����ܱ������У�������Ӧ��X(g)+Y(g)2Z(g)��H��0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
(1)��Ӧ0~2minZ��ƽ������v(Z)=____
(2)���жϸ÷�Ӧ�Ѿ��ﵽƽ��״̬����____
A������X������������Z�����ʵ�2�� B��������ѹǿ���ֲ���
C��������������ܶȱ��ֲ��� D�������ڸ������Ũ�ȱ��ֲ���
(3)�¶�Ϊ300��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��K�� ___
II��(1)�����£�0.005mol��L-1Ba(OH)2��Һ��pH��_____
(2)�����£���0.1mol��L-1NH3��H2O��Һ�в��ϼ�ˮ��������c(OH-)/c(NH3��H2O)��____(ѡ����������������С��������������
(3)�±��г��˼������������������������pH����ʼ������pH����������Ũ��Ϊ1.0mol��L-1���㣩
Fe3�� | Al3�� | Zn2�� | |
��ʼ������pH | 1.1 | 3.2 | 5.9 |
��ȫ������pH | 3.2 | 5 | 8.9 |
ij��Һ�к�Fe3����Al3����Zn2��������ȥFe3����Al3���������еμ�1.0moL��L-1��NaOH��Һ������Һ��pHΪ___��