题目内容
【题目】一些烷烃的燃烧热如下表:
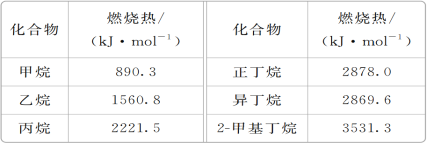
下列表达正确的是( )
A. 乙烷燃烧的热化学方程式为2C2H6(g)+7O2(g)===4CO2(g)+6H2O(g) ΔH=-1560.8 kJ·mol-1
B. 稳定性:正丁烷>异丁烷
C. 正戊烷的燃烧热大于3531.3 kJ·mol-1
D. 相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多
【答案】C
【解析】
A项,乙烷的燃烧热为1560.8kJ/mol,指1molC2H6(g)完全燃烧生成CO2(g)和H2O(l)放出1560.8kJ的热量,乙烷燃烧热表示的热化学方程式为C2H6(g)+![]() O2(g)=2CO2(g)+3H2O(l)ΔH=-1560.8kJ/mol,A项错误;
O2(g)=2CO2(g)+3H2O(l)ΔH=-1560.8kJ/mol,A项错误;
B项,正丁烷和异丁烷互为同分异构体,1mol正丁烷和异丁烷完全燃烧都生成4molCO2(g)和5molH2O(l),正丁烷的燃烧热>异丁烷的燃烧热,则正丁烷具有的能量>异丁烷具有的能量,根据能量越低越稳定,稳定性:正丁烷<异丁烷,B项错误;
C项,正戊烷和2—甲基丁烷互为同分异构体,根据正丁烷的燃烧热>异丁烷的燃烧热知,互为同分异构体的化合物支链多的燃烧热小,正戊烷的燃烧热>2—甲基丁烷的燃烧热,正戊烷的燃烧热大于3531.3kJ/mol,C项正确;
D项,随着碳原子数的增多烷烃含碳质量分数逐渐增大,1gCH4、C2H6、C3H8完全燃烧放出的热量依次为55.64kJ(![]() =55.64kJ)、52.03kJ(
=55.64kJ)、52.03kJ(![]() =52.03kJ)、50.49kJ(
=52.03kJ)、50.49kJ(![]() =50.49kJ),可见相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越少,D项错误;
=50.49kJ),可见相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越少,D项错误;
答案选C。

【题目】如图利用培养皿探究氨气的性质。实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面。下表中对实验现象所做的解释正确的是

选项 | 实验现象 | 解释 |
A | 浓盐酸附近产生白烟 | NH3与浓盐酸反应生成了NH4Cl固体 |
B | 浓硫酸附近无明显现象 | NH3与浓硫酸不发生反应 |
C | 氯化物溶液变浑浊 | 该溶液一定是AlCl3溶液 |
D | 干燥的红色石蕊试纸不变色,湿润的红色石蕊试纸变蓝 | NH3是一种可溶性碱 |
A. AB. BC. CD. D
【题目】Ⅰ、中和热的测定实验中取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于右图所示的装置中进行中和热的测定实验,回答下列问题:
(1) 从下图实验装置看,其中尚缺少的一种玻璃用品是__________。

温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | ||
H2SO4 | NaOH | 平均值 | ||
1 | 26.2 | 26.0 | 26.1 | 29.5 |
2 | 27.0 | 27.4 | 27.2 | 32.3 |
3 | 25.9 | 25.9 | 25.9 | 29.2 |
4 | 26.4 | 26.2 | 26.3 | 29.8 |
(2) 若0.55 mol/L NaOH溶液和0.25 mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃),通过以上数据计算中和热ΔH=_______( 结果保留小数点后一位)。
(3) 若改用60mL 0.25mol·L-1 H2SO4和50mL 0.55mol·L-1 NaOH溶液进行反应与上述实验相比,所放出的热量_______(填“相等”或“不相等”)
Ⅱ、在火箭推进器中装有还原剂肼(N2H4)和强氧化剂H2O2,当它们混合时即产生大量的氮气和水蒸气,并放出大量的热。已知0.4 mol液态肼和足量液态H2O2反应生成氮气和水蒸气时放出256.64 kJ的热量。写出肼和H2O2反应的热化学方程式:___________。
Ⅲ、(1)将pH=8的氢氧化钡溶液与pH=5的盐酸溶液混合并保持100℃恒温,欲使混合溶液的pH=7,则氢氧化钡溶液与盐酸的体积比为________。
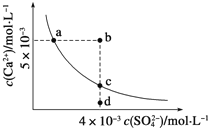
(2)已知AnBm的离子积K=[c(Am+)]n·[c(Bn-)]m,式中c(Am+)和c(Bn-)表示离子的物质的量浓度。在某温度下,氢氧化钙溶解度为0.74 g,其饱和溶液密度设为1 g·cm-3,其离子积为K=________。
【题目】用下图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是

选项 | ①中物质 | ②中物质 | 预测②中的现象 |
A. | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
B. | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
C. | 氯化铝溶液 | 浓氢氧化钠溶液 | 产生大量白色沉淀 |
D. | 草酸溶液 | 高锰酸钾酸性溶液 | 溶液逐渐褪色 |