题目内容
下列说法正确的是( )
| A、CO2分子的空间结构是直线形,故CO2分子是非极性分子 |
| B、分子CO和N2的原子总数相同,价电子总数相等,故性质相同 |
| C、Na+的电子排布式为1s22s22p63s1 |
| D、在元素周期表中,s区,d区和ds区的元素都是金属 |
考点:判断简单分子或离子的构型,元素周期表的结构及其应用,原子核外电子排布,极性分子和非极性分子
专题:原子组成与结构专题,元素周期律与元素周期表专题,化学键与晶体结构
分析:A、CO2分子中碳是sp杂化,所以空间结构是直线形,故CO2分子是极性键形成的非极性分子;
B、分子CO和N2的原子总数相同,价电子总数相等,两是等电子体,故结构相似;
C、Na+的电子排布式为1s22s22p6;
D、s区的氢不是金属.
B、分子CO和N2的原子总数相同,价电子总数相等,两是等电子体,故结构相似;
C、Na+的电子排布式为1s22s22p6;
D、s区的氢不是金属.
解答:
解:A、CO2分子中碳是sp杂化,所以空间结构是直线形,故CO2分子是极性键形成的非极性分子,故A正确;
B、分子CO和N2的原子总数相同,价电子总数相等,两是等电子体,故结构相似,故B错误;
C、Na+的电子排布式为1s22s22p6,故C错误;
D、s区的氢不是金属,故D错误;
故选A.
B、分子CO和N2的原子总数相同,价电子总数相等,两是等电子体,故结构相似,故B错误;
C、Na+的电子排布式为1s22s22p6,故C错误;
D、s区的氢不是金属,故D错误;
故选A.
点评:本题考查分子的空间构型和核外电子的排布,以及等电子的原理,比较简单.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
关于0.1mol/L Na2CO3溶液的叙述错误的是( )
| A、0.5L该溶液中钠离子的物质的量浓度为0.05mol/L |
| B、1L该溶液中含有Na2CO3的质量为10.6g |
| C、从1L该溶液中取出100mL,则取出溶液中Na2CO3的物质的量浓度为0.1mol/L |
| D、取该溶液10mL,加水稀释至100mL后,Na2CO3的物质的量浓度为0.01mol/L |
下列离子方程式中,不正确的是( )
| A、将氯气溶于水:Cl2+H2O═2H++Cl-+ClO- |
| B、AlCl3溶液中加入过量氨水:Al3++3NH3?H2O═Al(OH)3↓+3NH4+ |
| C、FeBr2溶液中通入过量的Cl2:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
| D、向Fe(NO3)2溶液中加入稀盐酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
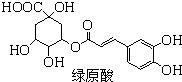 绿原酸是一种有降压作用的药物,可由咖啡酸(一种芳香酸)与奎尼酸通过酯化反应合成.下列说法正确的是( )
绿原酸是一种有降压作用的药物,可由咖啡酸(一种芳香酸)与奎尼酸通过酯化反应合成.下列说法正确的是( )| A、奎尼酸分子式为C9H8O4 |
| B、1mol奎尼酸与NaOH溶液反应,最多消耗5mol NaOH,1mol绿原酸与Br2水反应,最多消耗6mol Br2 |
| C、绿原酸能发生取代、加成、消去和还原反应 |
| D、咖啡酸和奎尼酸都能与FeCl3溶液发生显色反应 |
下列反应中,属于取代反应的是( )
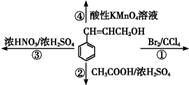

| A、①② | B、②③ | C、③④ | D、①④ |
下列化学药品的贮存方法正确的是( )
| A、新制氯水存放在带玻璃塞的无色细口瓶中 |
| B、镁条保存在细口瓶中密闭保存 |
| C、氢氧化钠固体保存在带橡胶塞的广口瓶中 |
| D、少量金属钠保存在煤油、四氯化碳等有机溶剂中 |
在1100℃,一定容积的密闭容器中发生反应:FeO(s)+CO(g)?Fe(s)+CO2(g)△H=a kJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法正确的是( )
| A、若增加CO的用量,上式中的△H增大 |
| B、若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
| C、若升高温度,则正反应速率加快,逆反应速率减慢,化学平衡正向移动 |
| D、达到化学平衡状态时,若c(CO)=0.100 mol/L,则c(CO2)=0.0263 mol/L |
下列说法不正确的是( )
| A、常温下,向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中:c(NH4+)=c(Cl-) |
| B、将等体积pH=4的盐酸和醋酸稀释成pH=5的溶液,醋酸所需加入的水量多 |
| C、pH=13的NaOH溶液与pH=1的醋酸溶液等体积混合后所得溶液的pH>7 |
| D、0.2mol?L-1的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(OH-)>c(H+) |
 A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图.请针对以下三种不同情况回答:
A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图.请针对以下三种不同情况回答: