题目内容
【题目】一定温度下,向一容积为2L的恒容密闭容器中充入2molA与3molB,在一定条件下反应:A(g)+B(g)C(g),△H >0,达到平衡后容器内压强是开始时的84%。若加入某种催化剂后反应的能量变化如图所示。下列说法正确的是( )
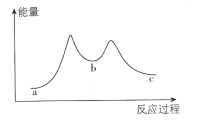
A.由图可知,加入催化剂之后,原反应分成了两步,第一步反应较慢
B.若40s后达到平衡,则用A表示该反应的速率为0.01molL-1min-1
C.当容器c(B)/c(A)不再改变时,不能说明该反应达到了平衡状态
D.达到平衡时,C的体积分数约为25%
【答案】A
【解析】
A.由图可知,加入催化剂之后,原反应分成了两步,第一步活化能大,因此第一步反应较慢,故A正确;
B.

2-x +3-x+x = 5×84% = 4.2
解得x = 0.8mol,若40s后达到平衡,则用A表示该反应的速率为![]() ,故B错误;
,故B错误;
C.容器![]() 的比值始终不改变,因此不能英语判断反应达到了平衡状态,故C错误;
的比值始终不改变,因此不能英语判断反应达到了平衡状态,故C错误;
D.达到平衡时,C的体积分数约为![]() ,故D错误。
,故D错误。
综上所述,答案为A。

【题目】废旧锂离子电池的正极材料试样(主要含有LiCoO2及少量Al、Fe等)可通过下列实验方法回收钴,并制备金属锂。
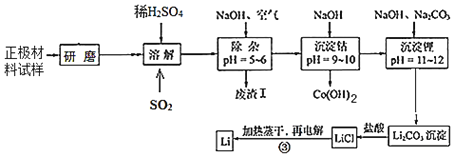
已知:①部分金属氢氧化物开始沉淀和完全沉淀时的pH:
氢氧化物 | Fe(OH)3 | Al(OH)3 | Co(OH)2 |
开始沉淀pH | 2.7 | 3.7 | 9.6 |
完全沉淀pH | 3.7 | 4.7 | 11 |
②Li2CO3在不同温度下的溶解度如下表:
温度/℃ | 0 | 10 | 20 | 50 | 75 | 100 |
Li2CO3的溶解度/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
(1)LiCoO2中,Co元素的化合价为_____。
(2)上述流程中为加快化学反应速率而采取的措施是_____。
(3)在上述溶解过程中,通入SO2的目的为_____。
(4)加NaOH调pH的目的是_____。
(5)写出“沉钴”过程中发生反应的离子方程式_____。
(6)洗涤所得Li2CO3沉淀要使用_____(填“热水”或“冷水”),将氯化锂溶液蒸干的过程中还需不断通入HCl气体,其作用是_____。
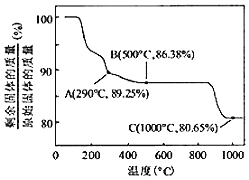
(7)Co(OH)2在空气中加热时,固体残留率随温度的变化如图所示。已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余固体的成分为_____(填化学式)。