题目内容
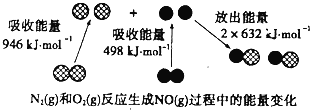
【题目】化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化.下列说法正确的是
A. 1molN2(g)和1molO2(g)反应放出的能量为180kJ
B. 通常情况下,N2(g)和O2混合能直接生成NO
C. NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
D. 1molN2(g)和1molO2(g)具有的总能量小于2molNO(g)具有的总能量
【答案】D
【解析】A、反应热就是断键吸收的能量和形成化学键所放出的能量的差值,所以该反应的反应热是946kJ/mol+498kJ/mol-2×632kJ/mol=+180kJ/mol,所以该反应是吸热反应,选项A不正确;B、氮气和氧气反应需要放电,选项B不正确;C、NO不是酸性氧化物,不能与氢氧化钠溶液反应,选项C不正确;D、反应物的总能量小于生成物的总能量的反应是吸热反应,根据A选项计算该反应是吸热反应,选项D正确。答案选D。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)![]() 2Z(g)△H<0,一段时间后达到平衡,反应过程中测定的数据如表:下列说法正确的是( )
2Z(g)△H<0,一段时间后达到平衡,反应过程中测定的数据如表:下列说法正确的是( )
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A. 该温度下此反应的平衡常数K=1.44
B. 其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正)
C. 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
D. 0~2min的平均速率ν(Z)=2.0×10﹣3molL﹣1min﹣1

