题目内容
【题目】青蒿素的一种化学合成方法的部分工艺流程如图所示: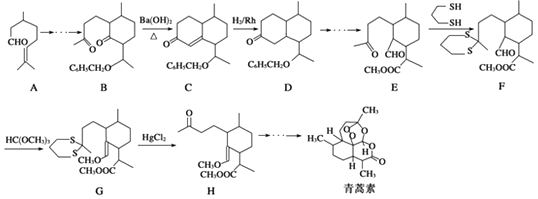
已知,羰基αH可发生下列反应: 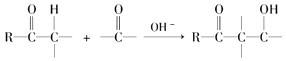 .
.
(1)化合物E中含有的含氧官能团有、和醛基.
(2)合成路线中设计E→F、G→H的目的是 .
(3)反应B﹣→C实际上可看作两步进行,依次发生的反应类型是、 .
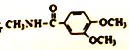
(4)A在Snβ沸石作用下,可生成同分异构体异蒲勒醇,已知异蒲勒醇分子中有3个手性碳原子,异蒲勒醇分子内脱水再与1分子H2加成可生成 ![]() ,则异蒲勒醇的结构简式为 .
,则异蒲勒醇的结构简式为 .
(5)写出以苯甲醛和乙烯为原料制备苄基乙醛( ![]() )的合成路线流程图(无机试剂任选).
)的合成路线流程图(无机试剂任选).
【答案】
(1)酯基,羰基
(2)保护羰基
(3)加成反应,消去反应
(4)![]()
(5)![]()
【解析】解:(1)根据E的结构可知,含有的含氧官能团为酯基、醛基、羰基;
(2)由E→F的结构可知,羰基中C=O双键变成C﹣S单键,由G→H的结构可知C﹣S单键又变成羰基,目的是保护羰基;
(3)由题目信息可知,结合B、C的结构可知,C=O双键变成C=C双键,应是B中连接羰基的甲基上的α﹣H与C=O先发生发生加成反应产生C﹣OH,再发生消去反应生成产生C=C双键生成C;
(4)由最终分子的结合,结合异蒲勒醇分子有3个手性碳原子、与A互为同分异构体,可知其结构为环状,分子内脱水,应含有﹣OH,根据A的结合可知﹣OH处于环中甲基的间位位置,结合加成产物 ![]() 可知应是异蒲勒醇与氢气发生1,4﹣加成,则异蒲勒醇的结构简式为:
可知应是异蒲勒醇与氢气发生1,4﹣加成,则异蒲勒醇的结构简式为: ![]() ;
;
(5)结合流程中B→C→D的变化分析设计,乙烯在催化剂加热条件下与水反应生成乙醇,乙醇催化氧化生成乙醛,乙醛与苯甲醛在氢氧化钡条件下生成 ![]() ,在氢气/Rh条件下发生加成反应生成
,在氢气/Rh条件下发生加成反应生成 ![]() ,
,
工艺流程图为: ![]() ;
;
所以答案是:(1)酯基、羰基;(2)保护羰基;(3)加成反应、消去反应;(4)![]() (5)
(5)![]()

【题目】元素是构成我们生活的世界中一切物质的“原材料”。
(1)自18世纪以来,科学家们不断探索元素之谜。通过从局部到系统的研究过程,逐渐发现了元素之间的内在联系。下面列出了几位杰出科学家的研究工作。
序号 | ① | ② | ③ | ④ |
科学 | 纽兰兹 | 道尔顿 | 德贝莱纳 | 尚古尔多 |
工作 | 发现“八音律”,指出从某一指定的元素起,第八个元素是第一个元素的某种重复 | 创立近代原子论,率先开始相对原子质量的测定工作 | 发现了5组性质相似的“三元素组”,中间元素的相对原子质量为前后两种元素相对原子质量的算术平均值 | 认为各元素组之间并非毫不相关,可以用相对原子质量把它们按从小到大的顺序串联 |
上述科学家的研究按照时间先后排序合理的是_________(填数字序号)。
(2)1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,如图所示。
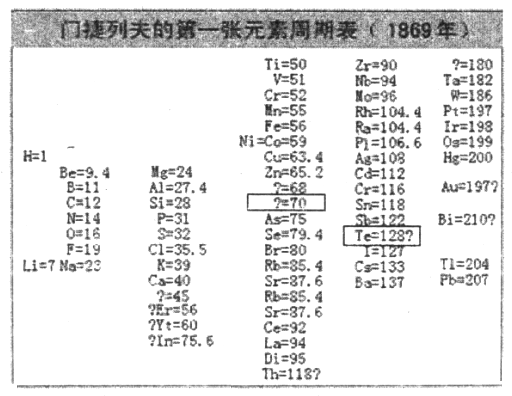
①门捷列夫将已有元素按照相对原子质量排序,同一___________(填“横行”或“纵列”)元素性质相似。结合表中信息,猜想第4列方框中“?=70”的问号表达的含义是_______________,第5列方框中“Te=128?”的问号表达的含义是_______________。
②到20世纪初,门捷列夫周期表中为未知元素留下的空位逐渐被填满。而且,随着原子结构的逐渐揭秘,科学家们发现了元素性质不是随着相对原子质量递增呈现周期性变化,而是随着原子序数(核电荷数)递增呈现周期性变化。其本质原因是_______________(填字母序号)。
A. 随着核电荷数递增,原子核外电子排布呈现周期性变化
B. 随着核电荷数递增,原子半径呈现周期性变化
C. 随着核电荷数递增,元素主要化合价呈现周期性变化
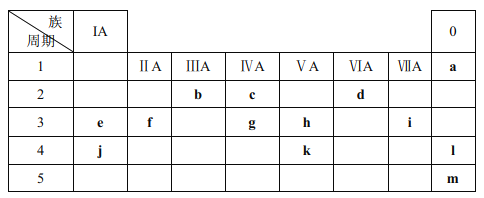
(3)短周期元素A、B、D、E、G、J在周期表中的位置如下:
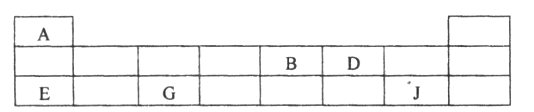
根据上表回答问题:
①D在周期表中的位置是_______________。
②A、B、E、G的原子半径由大到小的顺序是_______________(填元素符号)。
③B、D的气态氢化物的稳定性大小关系为_______________(填化学式)。
④E、G、J的最高价氧化物对应水化物两两之间反应的离子方程式分别为i. H++OH-=H2O、ii. _______________、iii_______________。
⑤用电子式表示E的最高价氧化物的形成过程_______________。