题目内容
【题目】下列关于热化学反应的描述中正确的是
A.HCl和NaOH反应的中和热ΔH=57.3kJ/mol,则H2SO4和Ba(OH)2反应的中和热ΔH=2×(57.3)kJ/mol
B.CO(g)的燃烧热是ΔH=283.0kJ/mol,则2CO(g)+O2(g)=2CO2(g)反应的ΔH=(2×283.0)kJ/mol
C.需要加热才能发生的反应一定是吸热反应
D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
【答案】B
【解析】
A.在稀溶液中,强酸跟强碱发生中和反应生成1 mol液态水时所释放的热量叫作中和热,H2SO4和Ba(OH)2反应除了生成水,还有硫酸钡沉淀生成,A错误;
B.CO(g)的燃烧热可用热化学方程式表示为:CO(g)+![]() O2(g)=CO2(g) ΔH=283.0 kJ/mol,B正确;
O2(g)=CO2(g) ΔH=283.0 kJ/mol,B正确;
C.任何反应发生都需要在一定条件下进行,在该过程中,断裂反应物化学键要吸收能量,产生的原子重新结合形成生成物时,产生新的化学键要释放能量,反应是放出热量还是吸收热量取决于断键吸收的能量与成键放出的能量差,所以反应过程的能量变化与反应条件无关,如C的燃烧反应,需要加热才能发生,C错误;
D.1mol甲烷完全燃烧热生成液态水和气态二氧化碳放出的热量为甲烷的燃烧热,D错误;
答案选B。

【题目】下列研究目的和示意图相符的是( )
① | ② | ③ | ④ | |
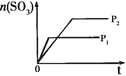
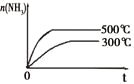
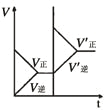
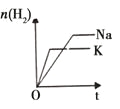
研 | 固定容积的密闭容器中,压强对反应: | 固定容积的密闭容器中,温度对反应: | 固定容积的密闭容器中,增大CO2浓度,对已达平衡的反应: | 等质量Na、K 分别与足量水反应 |
示 |
|
|
|
|
A. ①B. ②C. ③D. ④