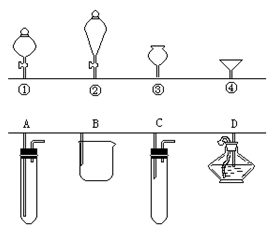
题目内容
下列实验操作能够达到实验目的的是( )
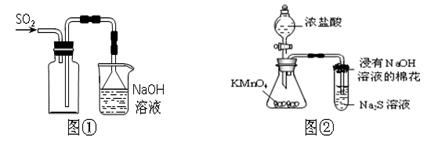

| A.实验室采用图①所示装置收集SO2 |
| B.可用图②所示装置比较KMnO4、Cl2、S的氧化性强弱 |
| C.实验室制取的溴乙烷中常含有少量溴,加适量的苯,振荡、静置后分液,可除去溴乙烷中的溴 |
| D.称取0.40 g NaOH,置于100 mL容量瓶中加水至刻度线,可配制0.10 mol/L NaOH溶液 |
B
考查常见的基本操作。SO2的密度大于空气的,应该是长口进,短口出,选项A不正确;溴乙烷和苯也是易溶的,不能作为萃取剂,选项C不正确;容量瓶不能用来溶解或稀释溶液,选项D不正确,因此正确的答案选B。

练习册系列答案
相关题目