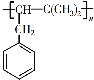题目内容
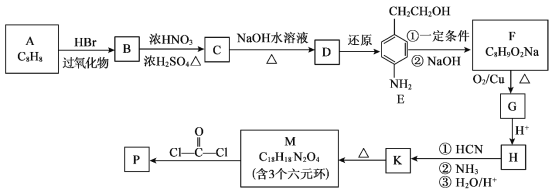
【题目】可降解聚合物P 的合成路线如下:
的合成路线如下:
已知: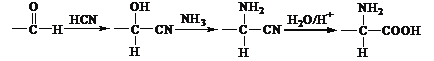
请回答:
(1)A为芳香烃,其结构简式为___________。
(2) E 中含氧官能团名称为 ___________。
(3) B→C 的反应类型为__________。
(4) C → D的方程式为________________。
(5) M 的结构简式为_______________ 。
(6)设计以A为原料,利用上述信息,合成高聚物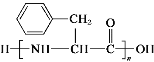 的路线: _____。( 用反应流程图表示,并注明反应条件 )
的路线: _____。( 用反应流程图表示,并注明反应条件 )
【答案】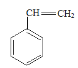 羟基 取代反应
羟基 取代反应 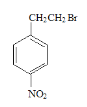 +NaOH
+NaOH![]()
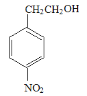 +NaBr
+NaBr 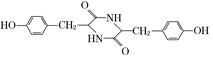
【解析】
A分子式是C8H8,为芳香烃,其不饱和度=![]() =5,则A为
=5,则A为 ,与HBr发生加成反应生成B,采用逆合成分析法易知,B为
,与HBr发生加成反应生成B,采用逆合成分析法易知,B为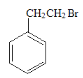 ,在浓硫酸作用下与浓硝酸发生硝化反应,生成C(
,在浓硫酸作用下与浓硝酸发生硝化反应,生成C( ),C在氢氧化钠水溶液条件下加热发生水解反应生成D(
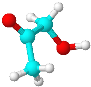
),C在氢氧化钠水溶液条件下加热发生水解反应生成D( ),D中硝基被还原为氨基转化为E,由F的分子式以及F到H的反应条件知,F中含有能催化氧化的醇羟基,还应含有酚钠结构,所以推出F的结构简式为
),D中硝基被还原为氨基转化为E,由F的分子式以及F到H的反应条件知,F中含有能催化氧化的醇羟基,还应含有酚钠结构,所以推出F的结构简式为![]() ,G为
,G为![]() ,H为
,H为![]() ,由信息ⅰ和ⅱ进一步推出K为
,由信息ⅰ和ⅱ进一步推出K为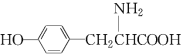 ,由M的分子式和M结构中含有3个六元环知,M由两分子K缩合得到,则M的结构简式为
,由M的分子式和M结构中含有3个六元环知,M由两分子K缩合得到,则M的结构简式为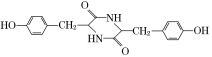 ,最后推出聚合物P为
,最后推出聚合物P为 ,据此分析作答。
,据此分析作答。
根据上述分析易知:
(1) A的结构简式为: ;
;
(2) E为 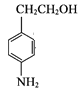 ,则其含氧官能团名称为羟基;
,则其含氧官能团名称为羟基;
(3)B为 ,在浓硫酸作用下与浓硝酸发生硝化反应,生成C(
,在浓硫酸作用下与浓硝酸发生硝化反应,生成C( ),则B→C 的反应类型为取代反应;
),则B→C 的反应类型为取代反应;
(4)C为 ,在氢氧化钠水溶液条件下加热发生水解反应生成
,在氢氧化钠水溶液条件下加热发生水解反应生成 ,故C → D的化学方程式为
,故C → D的化学方程式为 +NaOH
+NaOH![]()
 +NaBr;
+NaBr;
(5)依据上述分析可知,M 的结构简式为 ;
;
(6)根据上述已知合成路线可知,可先将苯乙烯与HBr发生加成反应得到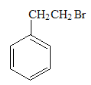 ,再进行水解反应生成
,再进行水解反应生成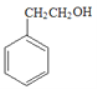 ,继续进行催化氧化得到
,继续进行催化氧化得到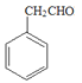 ,结合给定的信息ⅰ和ⅱ进一步反应得到单体
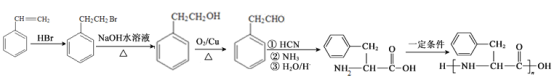
,结合给定的信息ⅰ和ⅱ进一步反应得到单体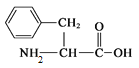 ,最后经过脱水缩合得到目标高聚物,其具体合成路线如下:
,最后经过脱水缩合得到目标高聚物,其具体合成路线如下:
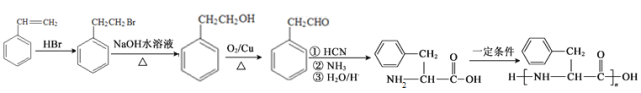

【题目】用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为2MnO![]() +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
实验序号 | A溶液 | B溶液 |
① | 20mL0.1mol·L-1H2C2O4溶液 | 30mL0.1mol·L-1KMnO4溶液 |
② | 20mL0.2mol·L-1H2C2O4溶液 | 30mL0.1mol·L-1KMnO4溶液 |
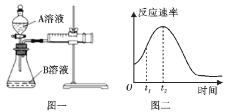
(1)该实验探究的是___因素对化学反应速率的影响。如图一,相同时间内针筒中所得的CO2体积大小关系是___(填实验序号)。
(2)若实验①在2min末收集了2.24mLCO2(标准状况下),则在2min末,c(MnO![]() )=___mol·L-1(假设混合液体积为50mL)。
)=___mol·L-1(假设混合液体积为50mL)。
(3)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定___来比较化学反应速率。
(4)小组同学发现反应速率总是如图二,其中t1~t2时间内速率变快的主要原因可能是:①产物MnSO4是该反应的催化剂、②___。
【题目】(10分)含碳物质的价值型转化,有利于“减碳”和可持续性发展,有着重要的研究价值。请回答下列问题:
(1)已知CO分子中化学键为C≡O。相关的化学键键能数据如下:
化学键 | H—O | C≡O | C=O | H—H |
E/(kJ·mol1) | 463 | 1075 | 803 | 436 |
CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH=___________kJ·mol1。下列有利于提高CO平衡转化率的措施有_______________(填标号)。
CO2(g)+H2(g) ΔH=___________kJ·mol1。下列有利于提高CO平衡转化率的措施有_______________(填标号)。
a.增大压强 b.降低温度
c.提高原料气中H2O的比例 d.使用高效催化剂
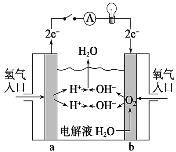
(2)用惰性电极电解KHCO3溶液,可将空气中的CO2转化为甲酸根(HCOO),然后进一步可以制得重要有机化工原料甲酸。CO2发生反应的电极反应式为________________,若电解过程中转移1 mol电子,阳极生成气体的体积(标准状况)为_________L。
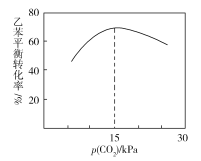
(3)乙苯催化脱氢制取苯乙烯的反应为:![]() (g)+CO2(g)
(g)+CO2(g)![]()
![]() (g)+CO(g)+H2O(g),其反应历程如下:
(g)+CO(g)+H2O(g),其反应历程如下:
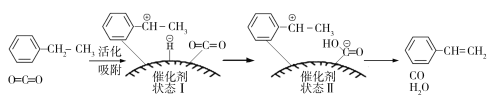
①由原料到状态Ⅰ____________能量(填“放出”或“吸收”)。
②一定温度下,向恒容密闭容器中充入2 mol乙苯和2 mol CO2,起始压强为p0,平衡时容器内气体总物质的量为5 mol,乙苯的转化率为_______,用平衡分压代替平衡浓度表示的化学平衡常数Kp=_______。[气体分压(p分)=气体总压(p总)×气体体积分数]
③乙苯平衡转化率与p(CO2)的关系如下图所示,请解释乙苯平衡转化率随着p(CO2)变化而变化的原因________________________________________________。