题目内容
【题目】将物质的量相等的硫酸铝和硫酸铵溶于水形成VmL混合溶液,向混合溶液中逐滴加入某氢氧化钠溶液(其物质的量浓度为混合溶液中两溶质的物质的量浓度之和),直至过量.下列表示氢氧化钠溶液加入的体积(x)与溶液中沉淀物的量(y)的关系示意图中正确的是( )
A. 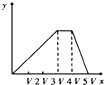 B.
B. 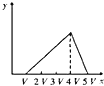
C. 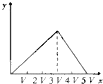 D.
D. 
【答案】A
【解析】假定含有Al2(SO4)3 ,(NH4)2 SO4的物质的量分别为1mol,反应顺序 :开始滴加NaOH发生为Al3++3OH-=Al(OH)3 ↓,沉淀逐渐增大,当Al3+沉淀完全时需加入6molOH-,生成Al(OH)3 2mol,达最大值;再发生NH4++OH-=NH3·H2O;NH4+完全反应时需2molOH-,该过程中沉淀氢氧化铝的量不变;最后继续加NaOH,发生反应Al(OH)3 +OH-=AlO2-+2H2O,直到2molAl(OH)3 溶解,需再加入2molNaOH。三段过程消耗NaOH的物质的量之比为6mol:2mol:2mol=3:1:1,三阶段消耗NaOH溶液的体积比为3:1:1。
A、从图象可知,开始滴加NaOH,即生成沉淀,达最大后,(铝离子完全反应)继续加NaOH,铵根离子开始反应,沉淀不变,当铵根离子反应完毕,氢氧根使氢氧化铝沉淀溶解,至最后消失,三阶段消耗NaOH溶液的体积比为3:1:1,图象A符合,故A正确;B、图为先与铵根离子反应,离子反应的顺序错误,故B错误;C、未考虑铵根离子的反应、氢氧化铝溶解消耗的氢氧化钠的物质的量不相符,故C错误;D、三阶段消耗NaOH溶液的体积比为3:1:1,图中比例为2:1:3不符合,故D错误。故选。

【题目】某兴趣小组用下图所示装置制备气体(酒精灯可以根据需要选择),对应说法正确的是

选项 | ①中药品 | ②中药品 | ③中药品 | ④中药品 | 制备气体 | ⑥中药品及作用 |
A | 浓盐酸 | MnO2 | 饱和食盐水 | 浓硫酸 | C12 | NaOH溶液,尾气吸收 |
B | 稀硝酸 | Cu | 烧碱溶液 | 浓硫酸 | NO | Na()H溶液,尾气吸收 |
C | 浓盐酸 | 大理石 | 饱和Na2CO3溶液 | 浓硫酸 | CO2 | 澄清石灰水,检验CO2 |
D | 浓盐酸 | Zn | 水 | 浓硫酸 | H2 | 可撤去 |
A. A B. B C. C D. D
