��Ŀ����
���ݻ��̶����ܱ������д������·�Ӧ��A(g)+3B(g) 2C(g)������ӦΪ���ȷ�Ӧ����ij�о�С���о���������������ʱ���ı�ijһ������������Ӧ��Ӱ�죬������ʵ�������������й�ϵͼ��
2C(g)������ӦΪ���ȷ�Ӧ����ij�о�С���о���������������ʱ���ı�ijһ������������Ӧ��Ӱ�죬������ʵ�������������й�ϵͼ��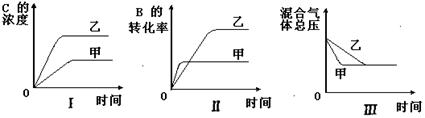
�����ж�һ��������ǣ� ��
| A��ͼI�о����Dz�ͬ�����Է�Ӧ��Ӱ�죬����ʹ�õĴ���Ч�ʽϸ� |
| B��ͼ���о�����ѹǿ�Է�Ӧ��Ӱ�죬�Ҽ�ѹǿ�ϸ� |
| C��ͼ���о������¶ȶԷ�Ӧ��Ӱ�죬�Ҽ��¶Ƚϸ� |
| D��ͼ���о����Dz�ͬ�����Է�Ӧ��Ӱ�죬�Ҽ�ʹ�õĴ���Ч�ʽϸ� |
AB
�����������������ֻ�ı仯ѧ��Ӧ��ʱ�䣬�Ի�ѧƽ����Ӱ�죬��A���������ѹǿ��ƽ����ϵ����С�ķ����ƶ�����B��ת����Ӧ�����ߡ��� B�����
���㣺��������Ի�ѧ��Ӧ���ʺͻ�ѧƽ���Ӱ��

̼�������(CH3OCOOC2H5)��һ�������﮵���л����Һ������̼���������ԭ��Ϊ��C2H5OCOOC2H5(g)+ CH3OCOOCH3(g)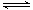 2 CH3OCOOC2H5(g)������������ͬ��CH3OCOOCH3��ƽ��ת����(��)���¶�(T)����Ӧ����ȣ�R=n(C2H5OCOOC2H5):n(CH3OCOOCH3)���Ĺ�ϵ����ͼ��ʾ�����ַ�Ӧ����ȷֱ�Ϊ1:1��2:1��3:1������˵������ȷ����( )
2 CH3OCOOC2H5(g)������������ͬ��CH3OCOOCH3��ƽ��ת����(��)���¶�(T)����Ӧ����ȣ�R=n(C2H5OCOOC2H5):n(CH3OCOOCH3)���Ĺ�ϵ����ͼ��ʾ�����ַ�Ӧ����ȷֱ�Ϊ1:1��2:1��3:1������˵������ȷ����( )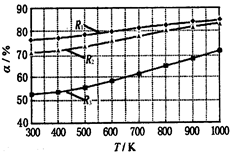
| A���÷�Ӧ��H > 0 |
| B��R1��Ӧ�ķ�Ӧ�����Ϊ3:1 |
| C��650�棬��Ӧ�����Ϊ1:1ʱ��ƽ�ⳣ��K = 6 |
| D���÷�ӦΪȡ����Ӧ |
��һ�ܱ������г���һ������N2��H2�����ⶨ��Ӧ��ʼ���2s�ڰ�����ƽ�����ʣ���(NH3)=0.3mol��(L��s������2sĩNH3��Ũ��Ϊ
| A��0.60mol��L | B��0.50mol��L | C��0.45mol��L | D��0.55mol��L |
��ͼ��ʾ��ӦA(g)+B(g) nC(g) ��H��0���ڲ�ͬ�����·�Ӧ�������C�İٷֺ����ͷ�Ӧ��������ʱ��Ĺ�ϵ���ߡ������й�������ȷ����
nC(g) ��H��0���ڲ�ͬ�����·�Ӧ�������C�İٷֺ����ͷ�Ӧ��������ʱ��Ĺ�ϵ���ߡ������й�������ȷ����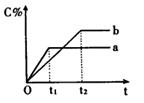
| A����Ӧ���淴Ӧ��ʼ |
| B��a��ʾ�д�����b��ʾ���� |
| C����n��2������������ͬ��a��b��ѹǿ�� |
| D��������������ͬ��a��b���¶ȸ� |
ij�ܱ������з������·�Ӧ��2X(g)��Y(g)  Z(g)����H <0 ��ͼ��ʾ�÷�Ӧ�����ʣ�v����ʱ�䣨t���仯�Ĺ�ϵͼ��t2��t3��t5ʱ��������������ı䣬����û�иı�����ʵ�������������˵���в���ȷ����
Z(g)����H <0 ��ͼ��ʾ�÷�Ӧ�����ʣ�v����ʱ�䣨t���仯�Ĺ�ϵͼ��t2��t3��t5ʱ��������������ı䣬����û�иı�����ʵ�������������˵���в���ȷ����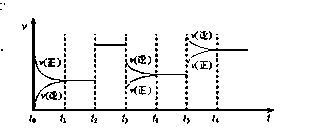
| A��t3ʱ��С��ѹǿ |
| B��t5ʱ������ѹǿ |
| C��t6ʱ�̺�Ӧ���ת������� |
| D��t1 - t2ʱ�÷�Ӧ��ƽ�ⳣ������t6 ʱ��Ӧ��ƽ�ⳣ�� |
 2HI��ƽ����ϵ����ѹ���ܱ���ϵ�еĻ�������ܶ�����
2HI��ƽ����ϵ����ѹ���ܱ���ϵ�еĻ�������ܶ����� eC(g)+fD(g)��Ӧ�����У���������������ʱ��C���������?(C)�ڲ�ͬ�¶�(T)�Ͳ�ͬѹǿ(P)����������ʱ��(t)�ı仯��ϵ��ͼ��ʾ������������ȷ���ǣ� ��
eC(g)+fD(g)��Ӧ�����У���������������ʱ��C���������?(C)�ڲ�ͬ�¶�(T)�Ͳ�ͬѹǿ(P)����������ʱ��(t)�ı仯��ϵ��ͼ��ʾ������������ȷ���ǣ� ��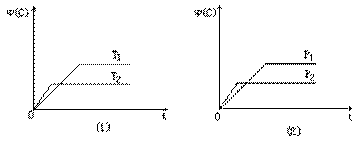
 C(g)��2D(g) ��H��0����һ�������´ﵽƽ�⣬�����й�������ȷ����
C(g)��2D(g) ��H��0����һ�������´ﵽƽ�⣬�����й�������ȷ���� CO(g) + Cl2(g) ��H>0 ����Ӧ�ﵽƽ��ʱ�����д�ʩ�������� �ں���ͨ��������� ������CO��Ũ�� �ܼ�ѹ �ݼӴ��� ��ѹͨ��������壬�����COCl2 �ֽ��ʵ���
CO(g) + Cl2(g) ��H>0 ����Ӧ�ﵽƽ��ʱ�����д�ʩ�������� �ں���ͨ��������� ������CO��Ũ�� �ܼ�ѹ �ݼӴ��� ��ѹͨ��������壬�����COCl2 �ֽ��ʵ���