ΧβΡΩΡΎ»ί
Ά≠ΒΞ÷ ΦΑΤδΜ·ΚœΈο‘ΎΙΛ“Β…ζ≤ζΚΆΩΤ―–÷–”–÷Ί“ΣΉς”ΟΓΘ
Θ®1Θ©“―÷ΣΘΚ2Cu2O(s) + O2(g) = 4CuO(s) ΓςHΘΫΘ≠292kJΓΛmolΘ≠1
2C(s)+O2(g) =2CO(g) ΓςHΘΫΘ≠221kJΓΛmolΘ≠1
«κ–¥≥ω”ΟΉψΝΩΧΩΖέΜΙ‘≠CuOΘ®sΘ©÷Τ±ΗCu2OΘ®sΘ©ΒΡ»»Μ·―ßΖΫ≥Χ ΫΘΚ ΘΜ
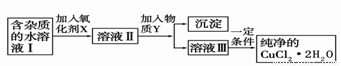
Θ®2Θ©œ÷”Ο¬»Μ·Ά≠ΨßΧε(CuCl2ΓΛ2H2OΘ§Κ§¬»Μ·―«Χζ‘”÷ )÷Τ»Γ¥ΩΨΜΒΡCuCl2ΓΛ2H2OΓΘœ»ΫΪΤδ÷Τ≥…Υ°»ή“ΚΘ§ΚσΑ¥»γΆΦ≤Ϋ÷ηΫχ––Χα¥Ω:
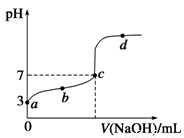
“―÷ΣCu2+ΓΔFe3+ΚΆFe2+ΒΡ«β―θΜ·ΈοΩΣ Φ≥ΝΒμΚΆ≥ΝΒμΆξ»Ϊ ±ΒΡpHΦϊœ¬±μ
Ϋπ τάκΉ” | Fe3+ | Fe2+[ά¥‘¥:―ß&ΩΤ& | Cu2+ |
«β―θΜ·ΈοΩΣ Φ≥ΝΒμ ±ΒΡpH | 1.9 | 7.0 | 4.7 |
«β―θΜ·ΈοΆξ»Ϊ≥ΝΒμ ±ΒΡpH | 3.2 | 9.0 | 6.7 |
«κΜΊ¥πœ¬Ν–Έ Χβ:
ΔΌœ÷”–―θΜ·ΦΝNaClOΓΔH2O2ΓΔKMnO4Θ§XΦ”ΡΡ÷÷ΚΟΘ§ΈΣ ≤Ο¥ΘΩ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘΜΗΟΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ ΓΘ
ΔΎ»ή“ΚII÷–≥ΐCu2+ΆβΘ§ΜΙ”–ΓΓΓΓΓΓΓΓΓΓΫπ τάκΉ”Θ§»γΚΈΦλ―ιΤδ¥φ‘Ύ ΓΘ
ΔέΈο÷ Y≤ΜΡήΈΣœ¬Ν–ΒΡ
aΘ°CuO bΘ°Cu(OH)2 cΘ°CuCO3 dΘ°Cu2(OH)2CO3 eΘ°CaO fΘ°NaOH
Δή»τœρ»ή“ΚΔρ÷–Φ”»κΧΦΥαΗΤΘ§≤ζ…ζΒΡœ÷œσ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘ
Θ®1Θ©C(s)ΘΪ2CuO(s)ΘΫCO(g)ΘΪCu2O(s) ΓςHΘΫ+35.5kJΓΛmolΘ≠1Θ®2Ζ÷Θ©
Θ®2Θ©ΔΌH2O2ΚΟΘ§≤Μ“ΐ»κ‘”÷ άκΉ”Θ®2Ζ÷Θ©ΓΘ
H2O2+2Fe2++2H+=2 Fe3++2H2OΘ®2Ζ÷Θ©
ΔΎFe3+Θ®1Ζ÷Θ©Θ§»Γ…ΌΝΩ»ή“Κ”Ύ ‘Ιή÷–Θ§ΒΈΦ”KSCN»ή“ΚΘ§»τ»ή“Κ±δΚλ…ΪΘ§÷ΛΟςΚ§Fe3+ΓΘ»τ»ή“Κ≤Μ±δΚλ…ΪΘ§‘ρ÷ΛΟς≤ΜΚ§Fe3+ΓΘΘ®2Ζ÷Θ©
ΔέefΘ®2Ζ÷Θ©
ΔήΧΦΥαΗΤ»ήΫβ,≤ζ…ζΤχ≈ίΚΆΚλΚ÷…Ϊ≥ΝΒμΘ®1Ζ÷Θ©
ΓΨΫβΈωΓΩ
‘ΧβΖ÷ΈωΘΚΘ®1Θ©άϊ”ΟΗ«ΥΙΕ®¬…Θ§
ΔΌ2Cu2O(s) + O2(g) = 4CuO(s) ΓςHΘΫΘ≠292kJΓΛmolΘ≠1
ΔΎ2C(s)+O2(g) =2CO(g) ΓςHΘΫΘ≠221kJΓΛmolΘ≠1
”ΟΔΎΘ≠ΔΌΩ…“‘ΒΟΒΫΘΚC(s)ΘΪ2CuO(s)ΘΫCO(g)ΘΪCu2O(s) ΓςHΘΫ+35.5kJΓΛmolΘ≠1Θ®2Ζ÷Θ©
Θ®2Θ©ΔΌΗΏΟΧΥαΦΊΚΆ¥Έ¬»ΥαΡΤΉς―θΜ·ΦΝΒΡΜΑΘ§ΕΦ“ΣΜα“ΐ»κ‘”÷ άκΉ”Θ§±ψ «H2O2 «¬Χ…Ϊ―θΜ·ΦΝΘ§≤Μ“ΐ»κ‘”÷ άκΉ”Θ®2Ζ÷Θ©ΓΘH2O2+2Fe2++2H+=2 Fe3++2H2OΘ®2Ζ÷Θ©ΔΎFe3+Θ®1Ζ÷Θ©Θ§»Γ…ΌΝΩ»ή“Κ”Ύ ‘Ιή÷–Θ§ΒΈΦ”KSCN»ή“ΚΘ§»τ»ή“Κ±δΚλ…ΪΘ§÷ΛΟςΚ§Fe3+ΓΘ»τ»ή“Κ≤Μ±δΚλ…ΪΘ§‘ρ÷ΛΟς≤ΜΚ§Fe3+ΓΘΘ®2Ζ÷Θ©Δέ»ή“ΚΔρ «Υα–‘»ή“ΚΘ§Φ”»κΚ§Ά≠ΒΡΈο÷ Ω…“‘ΒςΫΎ»ή“ΚΒΡpH÷ΒΘ§Ε‘”ΎefΕχ―‘Θ§Υδ»ΜΩ…“‘ΒςΫΎ»ή“ΚΒΡpH÷ΒΘ§ΒΪ «“ΐΫχΝΥ‘”÷ άκΉ”ΓΘΘ®2Ζ÷Θ©ΔήΧΦΥαΗΤ»ήΫβ,≤ζ…ζΤχ≈ίΚΆΚλΚ÷…Ϊ≥ΝΒμΘ®1Ζ÷Θ©
ΩΦΒψΘΚΩΦ≤ι»»Μ·―ßΘ§Έο÷ ΒΡΧα¥ΩΓΘ