题目内容
9.用NA表示阿伏伽德罗常数的数值,下列说法正确的是( )| A. | 0.1 mol•Lˉ1的醋酸溶液中CH3COOH和CH3COOˉ的总数为NA | |
| B. | 1 molNa2O2与足量H2O充分反应,转移的电子数为2NA | |
| C. | 39g苯中所含的碳碳双键为1.5 NA | |
| D. | 23g乙醇中所含的羟基数为0.5 NA |
分析 A、不知道溶液体积,无法求出微粒数目;
B、Na2O2~e-,据此计算转移的电子数;
C、苯中没有碳碳双键
D、一个乙醇分子中含有一个羟基.
解答 解:A、不知道溶液体积,无法求出0.1mol/L的醋酸钠溶液中含CH3COOH、CH3COO-粒子总数,故A错误;
B、1molNa2O2与足量H2O充分反应,转移的电子数为NA,故B错误;
C、苯中没有碳碳双键,故C错误;
D、23g乙醇是0.5mol,其中所含的羟基数为0.5 NA,故D正确;
故选D.
点评 本题考查了阿伏伽德罗常数,注意1mol过氧化钠发生氧化还原反应,转移的电子数是1mol,本题题量稍大,难度中等.

练习册系列答案
相关题目
19.设NA为阿伏加德罗常数,下列叙述正确的是( )
| A. | 5.4g Al分别与含溶质0.2 mol的NaOH溶液、盐酸反应,生成H2分子数均为0.3NA | |
| B. | 5.35g NH4Cl固体中含有的N-H键个数为0.4NA | |
| C. | 将含有1mol FeCl3的浓溶液全部制成胶体,含Fe(OH)3胶粒的数目为NA | |
| D. | 120g熔融的NaHSO4中含阳离子总数为2NA |
20.已知碳碳单键可以绕键轴自由旋转,结构简式为如图所示的烃,下列说法中不正确的是( )


| A. | 等质量的该烃和甲烷均完全燃烧,耗氧量前者小于后者 | |
| B. | 该烃能使酸性高锰酸钾溶液褪色,属于苯的同系物 | |
| C. | 分子中一定有11个碳原子处于同一平面上 | |
| D. | 该烃的一氯取代产物为5种 |
17.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 14 g C2H4中含有2NA个C-H键 | |
| B. | 1 mol•L-1 NH3•H2O溶液中含有NA个NH4+ | |
| C. | 1 mol Na2O2和足量CO2反应产生NA个O2分子 | |
| D. | 常温常压下,22.4 L 的SO2中含有NA个SO2分子 |
4.4月25日,尼泊尔发生8.1级地震,受灾地区震后急需从外地补充大量物资.下列物质是救灾物资的一部分,相关说法不正确的是( )
| A. | 葡萄糖氯化钠注射液--用于补充热能和体液 | |
| B. | 二氧氯(ClO2)或漂白粉--利用其氧化性对居所和饮用水消毒 | |
| C. | 络合碘--碘化钾的水溶液,可以用于皮肤和粘膜的消毒 | |
| D. | 电池--通常选用干电池,用于小功率电器的供电 |
14. 下图为根据电解原理制成“银电量计”.其原理是:通过测定电解过程中附着在惰性电极上金属质量,计算通过电解池的电量.下列说法正确的是( )
下图为根据电解原理制成“银电量计”.其原理是:通过测定电解过程中附着在惰性电极上金属质量,计算通过电解池的电量.下列说法正确的是( )
 下图为根据电解原理制成“银电量计”.其原理是:通过测定电解过程中附着在惰性电极上金属质量,计算通过电解池的电量.下列说法正确的是( )
下图为根据电解原理制成“银电量计”.其原理是:通过测定电解过程中附着在惰性电极上金属质量,计算通过电解池的电量.下列说法正确的是( )| A. | 电量计工作时溶液里的阴离子向正极移动 | |
| B. | 电量计工作时银棒应与电源的正极相连 | |
| C. | 网袋是收集银溶解过程中产生的金属颗粒,若没有该网袋,测量结果会偏低 | |
| D. | 若得金属银的沉积量为1.08g,则电解过程中转移的电子为0.01mol |
1.硫化氢的转化是资源利用和环境保护的重要研究课题.下列关于硫化氢的说法错误的是( )

| A. | H2S是一种弱电解质 | |
| B. | 可用石灰乳吸收H2S气体 | |
| C. | 根据如图可知FeCl3、CuCl2均能氧化H2S | |
| D. | H2S在空气中燃烧可以生成SO2 |
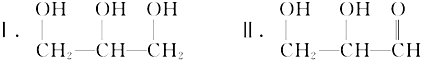
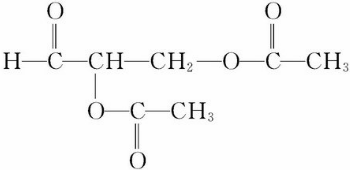 .
.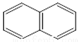 或
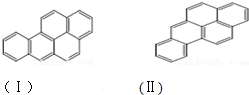
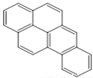
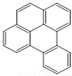
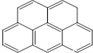
或 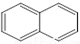 ,两者是等同的.苯并[α]芘是强致癌物质(存在于烟囱灰、煤焦油、燃烧的烟雾和内燃机的尾气中).它的分子由5个苯环并合而成,其结构可以表示为(Ⅰ)或(Ⅱ)式,这两者也是等同的:
,两者是等同的.苯并[α]芘是强致癌物质(存在于烟囱灰、煤焦油、燃烧的烟雾和内燃机的尾气中).它的分子由5个苯环并合而成,其结构可以表示为(Ⅰ)或(Ⅱ)式,这两者也是等同的: