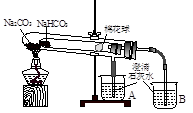��Ŀ����
��ҵ���Ի�ͭ��(��Ҫ�ɷ�CuFeS2)Ϊԭ���Ʊ�����ͭ�����������ֹ��ա�
I.����������:���������Ļ�ͭ�����ʯӢ����ͨ�˿������б��գ������Ƶô�ͭ��
��1�����յ��ܷ�Ӧʽ�ɱ�ʾΪ��2CuFeS2 + 2SiO2+5O2��2Cu+2FeSi03+4SO2�÷�Ӧ����������_____��
��2�����д���SO2�ķ���������������_____
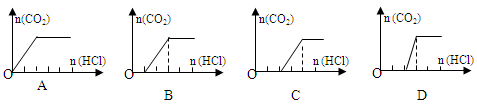
| A���߿��ŷ� |
| B���ô�����Һ�����Ʊ��������� |
| C���ð�ˮ���պ��پ������Ʊ������ |
| D����BaCl2��Һ�����Ʊ�BaSO3 |
A���ˣ�B�ӹ���NaOH��Һ��C�����ᾧ��D���գ�E��������
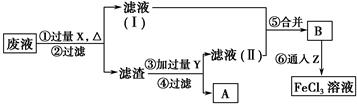
II.FeCl3��Һ��ȡ����:��������������ͼ��ʾ
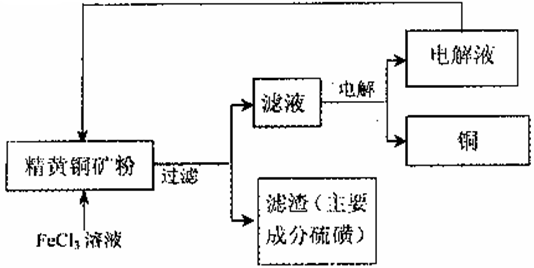
��4�����������У�CuFeS2��FeCl3��Һ��Ӧ�����ӷ���ʽΪ _____________��
��5���ù��������У�����ѭ�����õ�������_____(�ѧʽ)��
��6������ʯī�缫�����Һ��д�������ĵ缫��ʽ_____________��
��7����ͭ���к�����Pb,����C1һŨ�ȿɿ�����Һ��Pb2+��Ũ�ȣ���c(C1һ)��2mo1��L-1ʱ��Һ��Pb2+���ʵ���Ũ��Ϊ__mol��L-1��[��֪KSP(PbCl2)��1 x 10һ5]
��15�֣���1��CuFeS2��O2����1�֣���2�֣�
��2��A��D�����1����1�֣���������֣���2�֣�
��3��C��2�֣�
��4��CuFeS2+4Fe3+��Cu2++5Fe2++S��û��ƽ��1�֣���3�֣�
��5��FeCl3����2�֣�
��6��Fe2+��e����Fe3+����2�֣�
��7��2.5��10��6��2�֣�
���������������1�����ݷ���ʽ2CuFeS2 + 2SiO2+5O2��2Cu+2FeSiO3+4SO2��֪���ڷ�Ӧ������Ԫ�صĻ��ϼ۴ӣ�2�����ߵ�+4�ۣ�ʧȥ���ӣ����CuFeS2�ǻ�ԭ������������Ԫ�صĻ��ϼ۴�0�۽��͵���2�ۣ�ͭԪ�صĻ��ϼ۴ӣ�2�۽��͵�0�ۣ���˸÷�Ӧ����������CuFeS2��O2��
��2��A.SO2�Ǵ�����Ⱦ����������ŷţ�A����ȷ��B.�ô�����Һ�����Ʊ��������ƣ����Է�ֹ��Ⱦ��B��ȷ��C.�ð�ˮ���պ��پ������Ʊ�����泥�Ҳ���Է�ֹ��Ⱦ��C��ȷ��D.SO2���������Ȼ�����Һ�У������BaCl2��Һ�����Ʊ�BaSO3�Dz����ܵģ�D����ȷ����ѡAD��
��3��¯����Ҫ�ɷ���FeO ��Fe2O3 ��SiO2 ,Al2O3�ȣ�Ϊ�õ�Fe2O3�������ܽ����Ҫ���˳��������衣Ȼ���������������Һ�е����������������������ӣ��ټ������������������Һ�����������������������ˡ�ϴ�����ռ��õ�����������˺�������������,δ�漰���IJ����������ᾧ����ѡC��
��4�����˵õ�����ֽ�к������ʣ���˵��CuFeS2��FeCl3��Һ��������������ԭ��Ӧ�������ӽ���������������˷�Ӧ�����ӷ���ʽΪCuFeS2+4Fe3+��Cu2++5Fe2++S��
��5�����ʱ�����ĵ��Һ�ֿ������ͭ��Ӧ����˸ù��������У�����ѭ�����õ�������FeCl3��
��6������������ʧȥ���ӣ��������ʯī�缫�����Һ������������������ʧȥ���ӣ����������ĵ缫��ʽFe2+��e����Fe3+��
��7����֪KSP(PbCl2)��1��10һ5����˵���Һ��c(C1һ)��2mo1��L-1ʱ��Һ��Pb2+���ʵ���Ũ��Ϊ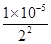 ��2.5��10��6mol��L-1��
��2.5��10��6mol��L-1��
���㣺����������ԭ��Ӧ�жϡ���������β����������ѧʵ����������Լ��绯ѧԭ����Ӧ�������

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д��������Ļ�����Ӧ�ù㷺����FeCl3������������ӡˢ��·ͭ�帯ʴ��������ֹѪ���ȡ�
��1��д��FeCl3��Һ��ʴӡˢ��·ͭ������ӷ���ʽ ��
| |
������Ӧ ������Ӧ ��
��3����ʴͭ���Ļ����Һ�У���Cu2����Fe3����Fe2����Ũ�Ⱦ�Ϊ
0.10mol��L��1��������±����������ݺ�ҩƷ��������ȥCuCl2��Һ��Fe3����Fe2����ʵ�鲽�� ��
| | �������↑ʼ����ʱ��pH | �������������ȫʱ��pH |
| Fe3�� Fe2�� Cu2�� | 1.9 7.0 4.7 | 3.2 9.0 6.7 |
| �ṩ��ҩƷ��Cl2 ŨH2SO4 NaOH��Һ CuO Cu | ||
��4��ij������Ա�������ʲ���������и�ʴ����������ijЩ����Һ�и�ʴ�������ԡ�����ϱ��ṩ��ҩƷ��ѡ�����֣�ˮ����ѡ����������ʵ�飬��֤���ʲ�����ױ���ʴ��
�йط�Ӧ�Ļ�ѧ����ʽ
���ʲ���ָ�ʴ��ʵ������
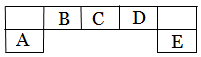
 ����������Ԫ��A��B��C��D��E��Ԫ�����ڱ��е�λ������ͼ��ʾ������AΪ�ؿ��к�����ߵĽ���Ԫ�ء�
����������Ԫ��A��B��C��D��E��Ԫ�����ڱ��е�λ������ͼ��ʾ������AΪ�ؿ��к�����ߵĽ���Ԫ�ء�