题目内容
 短周期主族元素A、B、C、D、E在元素周期表中的位置如下图所示,其中A为地壳中含量最高的金属元素。
短周期主族元素A、B、C、D、E在元素周期表中的位置如下图所示,其中A为地壳中含量最高的金属元素。
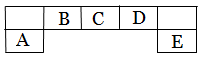
请用化学用语回答下列问题: (1)D元素在周期表中的位置:
(1)D元素在周期表中的位置:
(2)A、D 、E元素简单离子半径由大到小的顺序为_____>______ >______ (填微粒符号 ) (3)F与D同主族且相邻,其气态氢化物稳定性的大小 > (填微粒符号)
(3)F与D同主族且相邻,其气态氢化物稳定性的大小 > (填微粒符号)
(4)用高能射线照射含有10电子的D元素氢化物分子时,一个分子能释放一个电子,同时产生一种具有较高氧化性的阳离子,试写出该阳离子的电子式 ,该阳离子中存在的化学键有 。 (5)C元素的简单氢化物与E元素的最高价氧化物的水化物反应,生成化合物K,则K的水溶液显_____性(填“酸性”、“碱性”或“中性”),用离子方程式表示其原因 .
(5)C元素的简单氢化物与E元素的最高价氧化物的水化物反应,生成化合物K,则K的水溶液显_____性(填“酸性”、“碱性”或“中性”),用离子方程式表示其原因 .
(6) 化合物AC导热性好,热膨胀系数小,是良好的耐热冲击材料。其中制备AC的一种方法为:用A元素的氧化物、焦炭和C的单质在1600 ~ 1750℃生成AC,每生成1 mol AC,消耗18 g碳,吸收b kJ的热量。(热量数据为25℃、101.3 kPa条件下)写出该反应的热化学方程式 。
化合物AC导热性好,热膨胀系数小,是良好的耐热冲击材料。其中制备AC的一种方法为:用A元素的氧化物、焦炭和C的单质在1600 ~ 1750℃生成AC,每生成1 mol AC,消耗18 g碳,吸收b kJ的热量。(热量数据为25℃、101.3 kPa条件下)写出该反应的热化学方程式 。
(7)在Fe和Cu的混合物中加入一定量C的最高价氧化物的水化物稀溶液,充分反应后,剩余金属m1 g;再向其中加入稀硫酸,充分反应后,金属剩余 m2 g 。下列说法正确的是 。
a.加入稀硫酸前和加入稀硫酸后的溶液中肯定都有Cu2+
b.加入稀硫酸前和加入稀硫酸后的溶液中肯定都有Fe2+
c.m1一定大于m2
d.剩余固体m1 g 中一定有单质铜,剩余固体m2 g 中一定没有单质铜
(1)第二周期第ⅥA族(1分)
(2)Cl-> O2-> Al3+(2分) (3)H2O > H2S(1分)
(3)H2O > H2S(1分)
(4)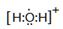 (1分) 极性共价键(1分)
(1分) 极性共价键(1分)
(5)酸性(1分) NH4+ + H2O  NH3·H2O + H+(2分)
NH3·H2O + H+(2分) (6)3C(s) + Al2O3(s) + N2 (g) =" 2AlN(s)" + 3CO(g) △H=" +2b" kJ/mol(3分)
(6)3C(s) + Al2O3(s) + N2 (g) =" 2AlN(s)" + 3CO(g) △H=" +2b" kJ/mol(3分)
(7)b、c(2分)
解析试题分析:根据题意知,A为地壳中含量最高的金属元素,则A为铝元素;结合常见元素在元素周期表中的位置判断:B为碳元素,C为氮元素,D为氧元素,E为氯元素。 (1)D为氧元素,在周期表中的位置:第二周期第ⅥA族;(2)A为铝元素;D为氧元素,E为氯元素;根据微粒半径比较原则判断,简单离子半径由大到小的顺序为Cl-> O2-> Al3+;
(1)D为氧元素,在周期表中的位置:第二周期第ⅥA族;(2)A为铝元素;D为氧元素,E为氯元素;根据微粒半径比较原则判断,简单离子半径由大到小的顺序为Cl-> O2-> Al3+; (3)F与氧同主族且相邻,则F为硫元素,同主族由上到下气态氢化物的稳定性逐渐减弱,其气态氢化物稳定性的大小H2O > H2S;(4)含有10电子的D元素氢化物分子为水分子,用高能射线照射水分子时,一个分子能释放一个电子,同时产生一种具有较高氧化性的阳离子,该阳离子的电子式见答案,该阳离子中存在的化学键有极性共价键;
(3)F与氧同主族且相邻,则F为硫元素,同主族由上到下气态氢化物的稳定性逐渐减弱,其气态氢化物稳定性的大小H2O > H2S;(4)含有10电子的D元素氢化物分子为水分子,用高能射线照射水分子时,一个分子能释放一个电子,同时产生一种具有较高氧化性的阳离子,该阳离子的电子式见答案,该阳离子中存在的化学键有极性共价键; (5)氮元素的简单氢化物与氯元素的最高价氧化物的水化物反应,生成化合物氯化铵,水溶液显酸性,用离子方程式表示其原因NH4+ + H2O
(5)氮元素的简单氢化物与氯元素的最高价氧化物的水化物反应,生成化合物氯化铵,水溶液显酸性,用离子方程式表示其原因NH4+ + H2O  NH3·H2O + H+;(6)
NH3·H2O + H+;(6) 根据题意知,氧化铝、焦炭和氮气在1600 ~ 1750℃生成氮化铝,每生成1 mol 氮化铝,消耗18 g碳,吸收b kJ的热量。(热量数据为25℃、101.3 kPa条件下)该反应的热化学方程式为3C(s) + Al2O3(s) + N2 (g) =" 2AlN(s)" + 3CO(g) △H=" +2b" kJ/mol;(7)在Fe和Cu的混合物中加入一定量硝酸稀溶液,由于铁的还原性比铜强,铁先与硝酸反应,充分反应后,生成硝酸亚铁,还可能有硝酸铜,剩余金属为铜或铁与铜的混合物,m1 g;再向其中加入稀硫酸,发生3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,或3Fe+2NO3-+8H+=3Fe2++2NO↑+4H2O,a.加入稀硫酸前和加入稀硫酸后的溶液中都不一定有Cu2+,错误;b.加入稀硫酸前和加入稀硫酸后的溶液中肯定都有Fe2+,正确;c.m1一定大于m2,正确;d.剩余固体m1 g 中一定有单质铜,剩余固体m2 g 中可能有单质铜,错误,选bc。
根据题意知,氧化铝、焦炭和氮气在1600 ~ 1750℃生成氮化铝,每生成1 mol 氮化铝,消耗18 g碳,吸收b kJ的热量。(热量数据为25℃、101.3 kPa条件下)该反应的热化学方程式为3C(s) + Al2O3(s) + N2 (g) =" 2AlN(s)" + 3CO(g) △H=" +2b" kJ/mol;(7)在Fe和Cu的混合物中加入一定量硝酸稀溶液,由于铁的还原性比铜强,铁先与硝酸反应,充分反应后,生成硝酸亚铁,还可能有硝酸铜,剩余金属为铜或铁与铜的混合物,m1 g;再向其中加入稀硫酸,发生3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,或3Fe+2NO3-+8H+=3Fe2++2NO↑+4H2O,a.加入稀硫酸前和加入稀硫酸后的溶液中都不一定有Cu2+,错误;b.加入稀硫酸前和加入稀硫酸后的溶液中肯定都有Fe2+,正确;c.m1一定大于m2,正确;d.剩余固体m1 g 中一定有单质铜,剩余固体m2 g 中可能有单质铜,错误,选bc。
考点:考查元素推断、元素周期律及相关物质的结构和性质,涉及电子式的书写、盐类水解、热化学方程式及硝酸的强氧化性。

 阅读快车系列答案
阅读快车系列答案(15分)硬质玻璃管是化学实验中经常使用的一种仪器,请分析下列实验(固定装置略)并回答问题。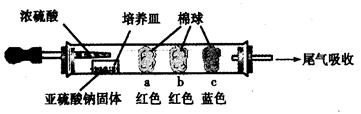
Ⅰ、进行微量实验:如图所示,将浓硫酸滴入装有Na2SO3固体的培养皿一段时间后,a、b、c三个棉球变化如下表。请填写表中的空白:
| 棉球 | 棉球上滴加的试剂 | 实验现象 | 解释和结论 |
| a | | 棉球变白,微热后又恢复红色 | |
| b | 含酚酞的NaOH溶液 | 棉球变为白色 | 离子方程式: |
| c | | 棉球变为白色 | 该气体具有 (选填“氧化性”或“还原性”) |
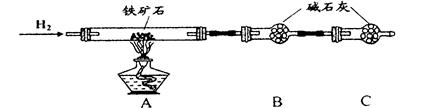
实验一:铁矿石中含氧量的测定
(1)按上图组装仪器(夹持仪器均省略),检查装置的气密性;
(2)将10.0g铁矿石放入硬质玻璃管中;
(3)从左端导气管口处不断地缓缓通入H2, 后,点燃A处酒精灯;
(4)充分反应后,撤掉酒精灯,再持续通入氢气至完全冷却。
(5)测得反应后装置B增重2.70g,则铁矿石中氧的质量分数为______________________。
实验二:铁矿石中含铁量的测定
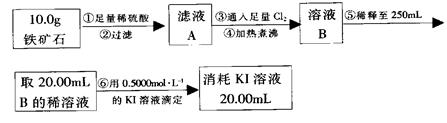
(1)步骤②和⑤中都要用到的玻璃仪器是 __。
(2)下列有关步骤⑥的操作中说法不正确的是_______。
A.滴定管用蒸馏水洗涤后再用待装液润洗
B.锥形瓶需要用待测液润洗
C.因为碘水为黄色,所以滴定过程中不需加指示剂
实验结论:推算铁的氧化物的组成,由实验一、二得出该铁矿石中铁的氧化物的化学式为
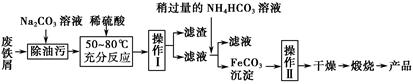
柠檬酸亚铁(FeC6H6O7)是一种易吸收的高效铁制剂,可由绿矾(FeSO4·7H2O)通过下列反应制备:
FeSO4+Na2CO3=FeCO3↓+Na2SO4
FeCO3+C6H8O7=FeC6H6O7+CO2↑+H2O
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Fe2+ | 5.8 | 8.8 |
(1)制备FeCO3时,选用的加料方式是 (填字母),原因是 。
a.将FeSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中
(2)生成的FeCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是 。
(3)将制得的FeCO3加入到足量柠檬酸溶液中,再加入少量铁粉,80 ℃下搅拌反应。①铁粉的作用是 。
②反应结束后,无需过滤,除去过量铁粉的方法是 。
(4)最后溶液经浓缩、加入适量无水乙醇、静置、过滤、洗涤、干燥,获得柠檬酸亚铁晶体。分离过程中加入无水乙醇的目的是 。
(5)某研究性学习小组欲从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3)出发,先制备绿矾,再合成柠檬酸亚铁。请结合下图的绿矾溶解度曲线,补充完整由硫铁矿烧渣制备FeSO4·7H2O晶体的实验步骤(可选用的试剂:铁粉、稀硫酸和NaOH溶液):向一定量烧渣中加入足量的稀硫酸充分反应, ,得到FeSO4溶液, ,得到FeSO4·7H2O晶体。

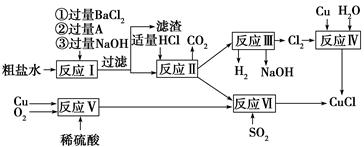
工业上以黄铜矿(主要成分CuFeS2)为原料制备金属铜,有如下两种工艺。
I.火法熔炼工艺:将处理过的黄铜矿加人石英,再通人空气进行焙烧,即可制得粗铜。
(1)焙烧的总反应式可表示为:2CuFeS2 + 2SiO2+5O2=2Cu+2FeSi03+4SO2该反应的氧化剂是_____。
(2)下列处理SO2的方法,不合理的是_____
| A.高空排放 |
| B.用纯碱溶液吸收制备亚硫酸钠 |
| C.用氨水吸收后,再经氧化制备硫酸铵 |
| D.用BaCl2溶液吸收制备BaSO3 |
A过滤;B加过量NaOH溶液;C蒸发结晶;D灼烧;E加氧化剂
II.FeCl3溶液浸取工艺:其生产流程如下图所示
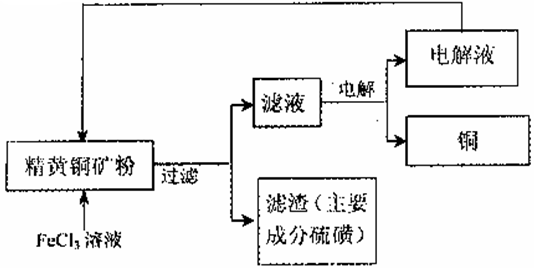
(4)浸出过程中,CuFeS2与FeCl3溶液反应的离子方程式为 _____________。
(5)该工艺流程中,可以循环利用的物质是_____(填化学式)。
(6)若用石墨电极电解滤液,写出阳极的电极反式_____________。
(7)黄铜矿中含少量Pb,调节C1一浓度可控制滤液中Pb2+的浓度,当c(C1一)=2mo1·L-1时溶液中Pb2+物质的量浓度为__mol·L-1。[已知KSP(PbCl2)=1 x 10一5]



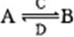 (在水溶液中进行)。其中C是产生温室效应的气体;D是淡黄色固体。写出C的结构式 ;D的电子式
(在水溶液中进行)。其中C是产生温室效应的气体;D是淡黄色固体。写出C的结构式 ;D的电子式