题目内容
【题目】在下列各溶液中,离子一定能大量共存的是( )
A. 室温下,pH=1的溶液中:Na+、Fe3+、NO![]() 、SO
、SO![]()
B. 含有0.1 mol·L-1 Fe3+的溶液中:K+、Mg2+、I-、NO![]()
C. 加入铝粉有气泡产生的溶液中:Na+、NH![]() 、Fe2+、NO
、Fe2+、NO![]()
D. 在AlCl3溶液中:K+、Na+、SiO![]() 、SO
、SO![]()
【答案】A
【解析】A、pH=1,说明溶液显酸性,这些离子能够大量共存,故A正确;B、Fe3+具有强氧化性,能把I-氧化成I2,不能大量共存,故B错误;C、加入Al能产生氢气,说明此溶液是酸或碱,如果是酸,NO3-具有强氧化性,能把Fe2+氧化成Fe3+,不能大量共存,如果是碱,不能与Fe2+大量共存,故C错误;D、Al3+和SiO32-发生双水解反应,不能大量共存,故D错误。

【题目】二氧化氯(ClO2)是极易溶于水且不与水发生化学反应的黄绿色气体,沸点为11℃,可用于处理含硫废水。某小组在实验室中探究ClO2与Na2S的反应。回答下列问题:
(1)ClO2的制备:
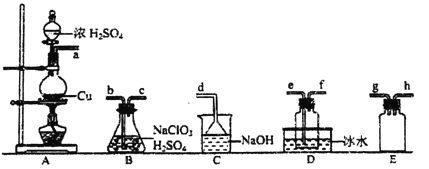
已知:SO2+2NaClO3+H2SO4=2ClO2↑+2NaHSO4
①装置A中反应的化学方程式为__________。
②欲收集ClO2,选择上图中的装置,其连接顺序为a→__________(按气流方向,用小写字母表示)。
③装置D的作用是___________________。
(2)C1O2与Na2S的反应

将上述收集到的ClO2用N2稀释以增强其稳定性,并将适量的稀释后的ClO2通入上图所示装置中充分反应,得到无色澄清溶液。一段时间后,通过下列实验探究I中反应的产物。
操作步骤 | 实验现象 | 结论 |
取少量I中溶液于试管甲中,滴加品红溶液和盐酸。 | 品红始终不褪色 | ①无_________生成 |
另取少量I中溶液于试管乙中,加入Ba(OH)2溶液,振荡 | ②____________ | 有SO42-生成 |
③继续在试管乙中滴加Ba(OH)2溶液至过量,静置,取上层清液于试管丙中,_______。 | 有白色沉淀生成 | 有Cl-生成 |
④ClO2与Na2S的反应的离子方程式为______________,用于处理含硫废水时,ClO2相对于Cl2的优点是_________________(任写一条)。