题目内容
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2H2O=H2SO4+2HBr相比较,水的作用不相同的是( )
| A.2Na2O2+2H2O=4NaOH+O2↑ | B.Cl2+H2O  HClO+HCl HClO+HCl |
| C.2F2+2H2O=4HF+O2 | D.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
C
解析试题分析:反应Br2+SO2+2H2O=H2SO4+2HBr中H2O既非氧化剂又非还原剂,A项、B项、C项中H2O也是既非氧化剂又非还原剂,作用相同。而C项2F2+2H2O=4HF+O2中H2O为还原剂,作用不同,故答案为C项。
考点:本题考查氧化还原反应。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
将一定质量的铜粉加入到100mL,某浓度的稀硝酸中充分反应后,容器中剩有m1g铜粉,此时共收集到NO气体448mL(标准状况) 。然后向上述混合物中加入稀硫酸至不再反应为止容器剩有铜粉m2g,则m1-m2为( )
| A.5.76 | B.2.88 | C.1.44 | D.4.32 |
在3S + 6KOH = 2K2S + K2SO3 + 3H2O 反应中,做氧化剂的S原子与做还原剂的S原子的物质的量之比是( )
| A.1:2 | B.2:1 | C.1:3 | D.3:1 |
下列变化中,必须加入氧化剂才能发生的是( )
| A.SO2→S | B.SO32-→SO2 | C.Fe2+→Fe3+ | D.HCO3-→CO32- |
根据表中信息,判断下列叙述中正确的是( )
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | / | | Cl- |
| ② | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
| ③ | KClO3 | 浓盐酸 | / | Cl2 | |
A.表中①组反应可能有一种或两种元素被氧化
B.氧化性强弱比较:KClO3>Fe3+>Cl2>Br2
C.表中②组反应的离子方程式是2MnO4-+3H2O2+6H+=2Mn2++4O2↑+6H2O
D.表中③组反应的还原产物是KCl,电子转移数目是6e-
3月22日是 “世界水日”。下列各反应中,水作为还原剂的是
A.2H2+O2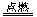 2H2O 2H2O | B.SO3+H2O=H2SO4 |
| C.2F2+2H2O=4HF+O2 | D.2Na+2H2O=2NaOH+H2↑ |
将0.39g锌粉加入到20.0 mL的0.200 mol·L-1 MO2+溶液中,恰好完全反应,则还原产物可能是
| A.M+ | B.M2+ | C.M3+ | D.MO42- |
实验室制取少量N2,常利用的反应是:NaNO2+NH4Cl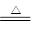 NaCl+N2↑+2H2O,关于该反应的说法正确的是
NaCl+N2↑+2H2O,关于该反应的说法正确的是
| A.NaNO2是氧化剂,发生还原反应 |
| B.生成1mol N2时转移的电子数为6mol |
| C.NH4Cl中的N元素被还原 |
| D.N2既是氧化剂又是还原剂 |
根据表中信息,判断下列叙述中正确的是
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | / | | Cl- |
| ② | KClO3 | 浓盐酸 | / | Cl2 | |
| ③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
B.氧化性强弱的比较:KClO3>Fe3+>Cl2>Br2
C.表中②组反应的还原产物是KCl,电子转移数目是6e-
D.表中③组反应的离子方程式为2MnO4-+3H2O2+6H+=2Mn2++4O2↑+6H2O