��Ŀ����
����Ŀ��CaS�������Ʊ������ᡢ������ë����ɱ���������ȣ�������ҽҩ��ҵ���ؽ��������������С�ij��ѧ̽��С����ʵ���������÷�Ӧ��
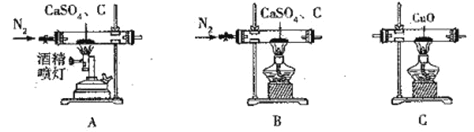
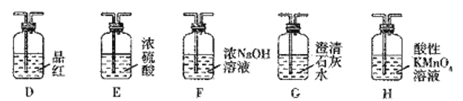
CaSO4+C![]() CaS+CaO+SO2��+CO��+CO2���Ʊ��Ʋ���������ѡ�õ�װ�����¡��ش��������⣺
CaS+CaO+SO2��+CO��+CO2���Ʊ��Ʋ���������ѡ�õ�װ�����¡��ش��������⣺
��֪:��C��E ~ H�е��Լ���Ϊ������
������KMnO4��Һ��������ʱ����Ԫ�ر���ԭ��Mn2+
��CaS��H2O��Ӧ����Ca(OH)2��H2S��
(1)ʵ��1����ֻ�������������Ƿ���CO���ɲ��õ�װ�����Ϊ______(��������������ĸ��ϣ����������д���CO��������________________________��
(2)ʵ��2����ֻ�������������Ƿ���CO2������õ����װ�����Ϊ______(��������������ĸ��ϣ�����ȥSO2�����ӷ���ʽΪ__________________________��
(3)ʵ��3����ͬʱ����CO2��SO2�����õ�װ�����Ϊ_______ (��������������ĸ��ϣ���
(4)���Ʊ���Ӧ��������ȫ��ͬ��������������ȫ��ͨ������ʵ��װ���У��õ����й��������±�:
ʵ��ǰ | ʵ��� | |
ʵ��1 | װ��CӲ�ʲ�������ͬCuO����Ϊ26.80 g | װ��CӲ�ʲ�������ͬ��Ӧ���������Ϊ26.64 g |
ʵ��2 | װ��G��ͬ��Һ����Ϊ187.50g | װ��G��ͬ��Ӧ����Һ������������Ϊ188.38 g |
ʵ��3 | װ��D��H��ͬ��Һ������Ϊ373.60g | װ��D��H��ͬ��Һ������Ϊ374.24 g |
д��CaSO4�ͽ�̿�ڸ��������·�Ӧ����CaS�Ļ�ѧ����ʽ��_______________��
(5)Ϊ��֤���ƵĻ�ѧʽ�������ʵ�飺��һ������(m1)����Ʒ���������ı���Na2CO3��Һ�У�ͨ��____�������Ƶù�������Ϊm2�����ʾ����ɵļ���ʽΪn(Ca):n(S)=__________(�ú�m1 ��m2�Ĵ���ʽ��ʾ)��
���𰸡�(1) AFECG(дAFGECG��AFEC��ACҲ�ɣ�2�֣� װ��C�к�ɫ�����Ϊ��ɫ��װ��G�г���ʯ��ˮ����ǣ�����һ��δѡGװ�ã�ֻ��д��װ��C������2�֣� (2) AHG 5SO2+2MnO4-+2H2O==2Mn2++5SO42-+4H+ (3)ADHG��AHG (4)2CaSO4+3C![]() CaS + CaO + SO2��+2CO2��+CO�� (5)���ˡ�ϴ�ӡ����ֻ����˸�1�֣���2�֣�
CaS + CaO + SO2��+2CO2��+CO�� (5)���ˡ�ϴ�ӡ����ֻ����˸�1�֣���2�֣� ![]()
�����������⿼��ʵ����Ʒ��������ۣ���1��CaSO4��C��Ӧ�����Ǹ��£���Ӧװ��ѡ��A��ֻ����CO������CO��ԭ����ͭ��Ȼ�������������CO2��CaSO4��C��Ӧ����CO2��SO2������������Ժ���ʵ��������ţ������ȥ����A��F����Ҫ����CO2��SO2�Ƿ���ȫ��������F��G��E��Ȼ��CO��ԭCuO��Ȼ��ͨ�����ʯ��ˮ��ǰ�߳���ʯ��ˮ������ǣ�װ��C�к�ɫ��Ϊ��ɫ�����߳���ʯ��ˮ����ǣ�˵�������к���CO������˳����A��F��G��E��C��G����2��SO2��CO2����ʹ����ʯ��ˮ����ǣ����ȳ�ȥSO2������SO2�Ļ�ԭ�ԣ�ͨ�����Ը��������Һ��Ȼ����ͨ�����ʯ��ˮ������ʯ��ˮ����ǣ�˵����CO2���ɣ����˳����A��H��G�������Ը��������Һ��Ӧ�����ӷ���ʽΪ��5SO2+2MnO4��+2H2O=2Mn2��+5SO42��+4H�� ����3����ΪCO2��SO2����ʹ����ʯ��ˮ����ǣ�����ȼ���SO2����������SO2�Ļ�ԭ�Ի�Ư���ԣ��������SO2�Ļ�ԭ�ԣ�A��H�����Ը��������Һ��ȥ��֤��SO2�Ĵ��ڣ�Ȼ����ͨ�����ʯ��ˮ������ʯ��ˮ����ǣ�˵����������CO2��װ��˳����A��H��G���������SO2��Ư���ԣ�Ӧͨ��Ʒ����Һ��Ʒ����Һ��ɫ��˵��SO2�Ĵ��ڣ���ͨ�뵽���Ը��������Һ�У�Ŀ���dz�ȥSO2�����ͨ�����ʯ��ˮ������ʯ��ˮ����ǣ�˵�������л���CO2��˳����A��D��H��G����4������ʵ��1��װ��C�з���CO��CuO=CO2��Cu��װ��C��Ӧǰ������������(26.8��26.64)g=0.16g�� ���ݲ����������CO�����ʵ���Ϊ0.16/16mol=0.01mol��ʵ��2��װ��G������������CO2�����ص���CO2����������Ϊ(188.38��187.50)g=0.88g����0.88/44mol=0.02mol��ʵ��3��װ��D��G�Ǽ��������SO2�����ص�����ΪSO2����������Ϊ(374.24��373.60)g=0.64g����0.64/64mol=0.01mol�����SO2��CO2��CO�����ʵ���֮��Ϊ0.01��0.02��0.01=1��2��1�������������ϵ��Ϊ1��2��1������ԭ���غ㣬�˷�Ӧ����ʽΪ2CaSO4��3C![]() CaS��CaO��SO2����2CO2����CO������5�����뱥��̼������Һ�������ij�����CaCO3����Ҫ���ˡ�ϴ�ӡ�������������ݸ�Ԫ���غ㣬������n(Ca2��)=m2/100mol������������ʵ���Ϊ(m1��
CaS��CaO��SO2����2CO2����CO������5�����뱥��̼������Һ�������ij�����CaCO3����Ҫ���ˡ�ϴ�ӡ�������������ݸ�Ԫ���غ㣬������n(Ca2��)=m2/100mol������������ʵ���Ϊ(m1��![]() )/32mol���������ʵ���֮��Ϊ
)/32mol���������ʵ���֮��Ϊ![]() ��
��

����Ŀ�������£���һԪ��HA����Һ��KOH��Һ��������(��������仯)
ʵ���� | ��ʼŨ��/(mol��L��1) | ��Ӧ���� Һ��pH | |
c(HA) | c(KOH) | ||
�� | 0.1 | 0.1 | 9 |
�� | x | 0.2 | 7 |
�����жϲ���ȷ����
A. ʵ��ٷ�Ӧ�����Һ�У�c(K��)>c(A��)>c(OH��)>c(H��)
B. ʵ��ٷ�Ӧ�����Һ�У�c(OH��)��c(K��)��c(A��)��![]() mol/L
mol/L
C. ʵ��ڷ�Ӧ�����Һ�У�c(A��)��c(HA)>0.1 mol/L
D. ʵ��ڷ�Ӧ�����Һ�У�c(K��)��c(A��)>c(OH��)��c(H��)