��Ŀ����
����Ŀ����2015���վ������⻯�ƣ�NaBH4���ڻ��������������Ҫ��Ӧ�ü�ֵ��ij�о�С�����ƫ������NaBO2Ϊ��Ҫԭ���Ʊ�NaBH4�����������£�
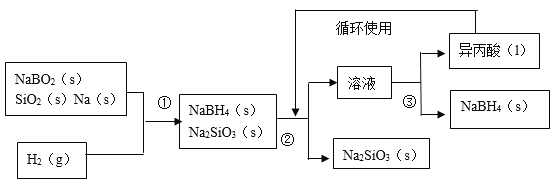
��֪��NaBH4����������ˮ��Ӧ������������ᣨ�е㣺13������
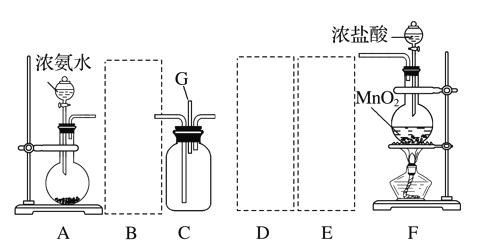
��1���ڵ�������Ӧ����֮ǰ����Ҫ����Ӧ��������100�����ϲ�ͨ��������ò�����Ŀ����_____��ԭ���еĽ�����ͨ��������____�У�ʵ����ȡ��������������Ҫ�õ���ʵ����Ʒ��_____��_____������Ƭ��С���ȡ�
��2������ƽ��������Ӧ�Ļ�ѧ����ʽ��
��NaBO2+��SiO2+��Na+��H2==��NaBH4+��Na2SiO3
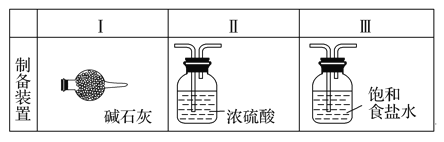
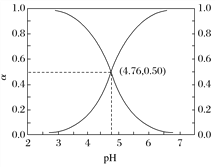
��3��������������õķ�����______�����������루NaBH4���������ܼ������õķ�����______��
��4��NaBH4��s����ˮ��l����Ӧ����NaBO2��s����������g������25����101KPa�£���֪ÿ����3.8��NaBH4��s������21.6KJ���÷�Ӧ���Ȼ�ѧ����ʽ��_______��
���𰸡���1����ȥ��Ӧ���е�ˮ�����Ϳ�����ú�ͣ����ӡ���ֽ��2��ϵ��Ϊ��1��2��4��2����3�����ˣ�����4��NaBH4��s��+H2O(l) = NaBO2��s��+H2(g) ��H=-216KJ/mol��
����������1������NaBH4����������ˮ��Ӧ����Na�Ƚϻ��ã����ȵ�100�����ϣ�����������dz�ȥ��
Ӧ���е�ˮ�����Ϳ���������Ӱ�췴Ӧ�����������Ʊ�����ú���ȡ����ʱ�������Ӽ�ȡ����ֽ��
�ɱ����ú�ͣ���2������������ԭ��Ӧԭ������ʧ��������ͬ��������ƽ�˷�ӦΪ��NaBO2+2SiO2+4Na+2H2==NaBH4+2Na2SiO3����3��������ͼ�п��Կ���������������ǹ����Һ���������ѡ�ù��˵ķ��������������루NaBH4���������ܼ���ֻ���Ƚ��ܼ��������������գ�������ķ������룻��4���������ʵ������㣬n(NaBH4)=0.1mol�����ȷ���ʽΪ��NaBH4��s��+H2O(l) = NaBO2��s��+H2(g) ��H=-216KJ/mol��

 ����ȫ���ִʾ��ƪ��ϵ�д�
����ȫ���ִʾ��ƪ��ϵ�д� �����߿����ϵ�д�
�����߿����ϵ�д� �㾦�½̲�ȫ�ܽ��ϵ�д�
�㾦�½̲�ȫ�ܽ��ϵ�д�