题目内容
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 1mol乙醇分子中含有极性键的数目为8NA
B. 80℃时,1LpH=1的硫酸溶液中,含H+的数目为0.2NA
C. Na2O2与2.24LCO2完全反应,转移电子的数目为0.1NA
D. 1molH2和1molI2于密闭容器中充分反应后,其分子总数目为2NA
【答案】D
【解析】分析:A、根据乙醇的结构分析;
B、根据氢离子浓度与pH的关系计算;
C、二氧化碳不一定处于标准状况下;
D、根据反应前后体积不变解答。
详解:A、乙醇的结构简式为CH3CH2OH,因此1mol乙醇分子中含有极性键的数目为7NA,A错误;
B、80℃时,1LpH=1的硫酸溶液中氢离子浓度是0.1mol/L,含H+的数目为0.1NA,B错误;
C、2.24LCO2不一定是0.1mol,Na2O2与2.24LCO2完全反应,转移电子的数目不一定为0.1NA,C错误;
D、1molH2和1molI2于密闭容器中充分反应:H2(g)+I2(g)![]() 2HI(g),因此反应后其分子总数目为2NA,D正确。答案选D。
2HI(g),因此反应后其分子总数目为2NA,D正确。答案选D。

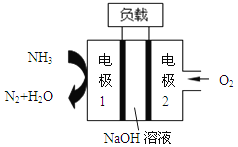
【题目】碳是自然界中形成化合物种类最多的元素,CO和CO2是碳的最常见氧化物。
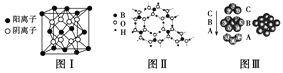
(1)研究和解决二氧化碳捕集和转化问题是当前科学研究的前沿领域。在太阳能的作用下,缺铁氧化物[Fe0.9O]能分解CO2,其过程如图1所示。过程①的化学方程式是______。在过程②中每产生0.1molO2,转移电子______mol。

(2)在催化剂作用下,将二氧化碳和氢气混合反应生成甲烷,是目前科学家们正在探索的处理空气中的二氧化碳的方法之一。
①已知:
共价键 | C=O | H—H | C—H | O—H |
键能/(kJmol-1) | 745 | 436 | 413 | 463 |
则CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) △H=______kJmol-1。
CH4(g)+2H2O(g) △H=______kJmol-1。
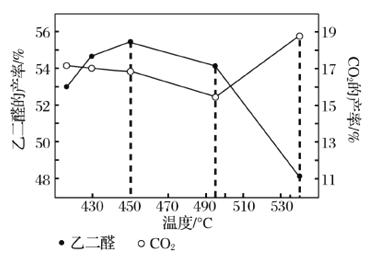
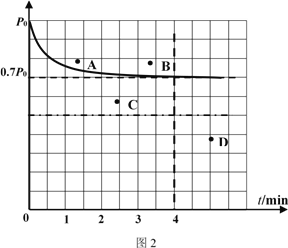
②向1L固定容积的密闭容器中加入4.0 mol H2(g)、1.0mol CO2,控制条件(催化剂:铑—镁合金、高温T1)使之反应,若测得容器内气体的压强随着时间的变化如图2所示。则4 min时容器内气体的密度为______;温度T1 下,该反应的化学平衡常为______。若采用2 L固定容积的密闭容器,投料量、催化剂和反应温度均保持不变,则反应重新达到平衡时对应体系内的压强的点是______(填字母)。
(3)工业合成原料气CO会与设备、管道及催化剂表面的金属铁、镍反应,生成羰基化合物。四羰基镍是热分解法制备高纯镍的原料,也是有机合成中供给一氧化碳的原料,还可做催化剂。Ni(s)+4CO(g)![]() Ni(CO)4(g) △H<0 Ni(CO)4(g)
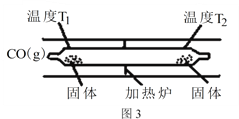
Ni(CO)4(g) △H<0 Ni(CO)4(g)![]() Ni(s)+4CO(g)。如图3所示,在石英真空管的温度为T1一端,放入少量粗镍和CO(g),一段时间后,在温度为T2的一端可得到纯净的镍。则温度T1______T2(填“>”“<”或“=”),上述反应体系中循环使用的物质为______(填化学式)。
Ni(s)+4CO(g)。如图3所示,在石英真空管的温度为T1一端,放入少量粗镍和CO(g),一段时间后,在温度为T2的一端可得到纯净的镍。则温度T1______T2(填“>”“<”或“=”),上述反应体系中循环使用的物质为______(填化学式)。
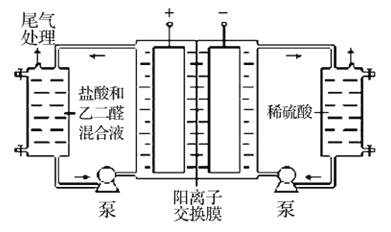
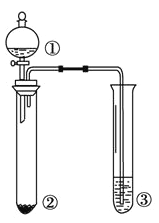
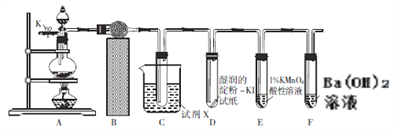
【题目】利用下图所示装置进行下列实验,能得出相应实验结论的是
选项 | ① | ② | ③ | 实验结论 |
|
A | 浓氯水 | NaBr | 淀粉KI溶液 | 氧化性:Cl2>Br2>I2 | |
B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
C | Br2的苯溶液 | 铁屑 | AgNO3溶液 | 苯与溴单质在铁催化剂作用下 发生取代反应 | |
D | 硝酸 | Na2SO3 | KMnO4溶液 | SO2能使KMnO4溶液褪色 |
A. A B. B C. C D. D