题目内容
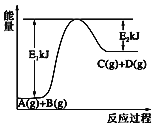
【题目】(1)已知2H→H2放出437.6 kJ的热量,下列说法正确的是____
A.氢气分子内每个氢原子都达到稳定结构
B.氢气分子的能量比两个氢原子的能量低
C.1molH2离解成 2 mol H 要放出437.6 kJ热量
D.氢原子比氢气分子稳定
(2)科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术2H2O![]() 2H2↑+O2↑。制得的氢气可用于制作燃料电池.试回答下列问题:
2H2↑+O2↑。制得的氢气可用于制作燃料电池.试回答下列问题:
①分解海水时,实现了光能转化为__能;生成的氢气用于制作燃料电池时,实现了化学能转化为____能;分解海水的反应属于___反应(填“放热”或“吸热”)
②某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,A极上发生的电极反应为:2H2+2O24e=2H2O,则B极的电极反应式为:____
(3)已知某电池的总反应为:Zn+2MnO2+2NH4Cl=ZnCl2+2NH3↑+Mn2O3+H2O,写出该电池的电极反应方程式:负极_______正极_______
【答案】AB 化学 电 吸热 O2 +4e =2O2 负极:Zn – 2e = Zn2+ 正极:2NH4+ +2MnO2+ 2e=2NH3↑+Mn2O3+H2O
【解析】
(1)A、氢气分子内每个氢原子都达到2电子稳定结构,选项A正确;
B、2molH结合成1molH2放出能量,则H2分子的能量比两个H原子的能量低,选项B正确;
C、根据已知2H→H2并放出437.6kJ的热量,所以1molH2离解成2molH要吸收437.6kJ的热量,选项C错误;
D、原子比分子能量高,氢气分子稳定,选项D错误;
答案选AB;
(2)①利用太阳能产生激光分解海水时,实现了光能转化为化学能;生成的氢气用于制作燃料电池时,化学能又转化为电能;分解海水的反应属于吸热反应;
②某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,A极上发生的电极反应为2H2+ 2O2- -4e-=2H2O,该反应为氧化反应,则A极是电池的负极,电子从该极流出,B极为正极,发生还原反应,电极反应式为O2+4e-=2O2-;
(3)在反应中Zn元素化合价升高,被氧化,Zn为负极反应,负极电极反应式为Zn – 2e = Zn2+,Mn元素化合价降低,被还原,MnO2为正极反应,正极反应式为2NH4+ +2MnO2+ 2e=2NH3↑+Mn2O3+H2O。