题目内容
A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图为: ,B最外层电子数是2,C的气态氢化物的水溶液呈碱性,据此填空:
,B最外层电子数是2,C的气态氢化物的水溶液呈碱性,据此填空:
(1)A的元素名称为________,其气态氢化物的稳定性比CH4________(填“强”或“弱”)。
(2)C、D的最高价氧化物的水化物的酸性大小为________>________(填化学式)。
(3)B的活泼性比钙的________(填“强”或“弱”)。
(1)硅 弱 (2)HNO3 H3PO4 (3)弱
解析

有A、B、C、D、E、F六种元素,已知:
①它们位于三个不同短周期,核电荷数依次增大。
②E元素的电离能数据见下表(kJ·mol-1):
| I1 | I2 | I3 | I4 | … |
| 496 | 4 562 | 6 912 | 9 540 | … |
③B与F同主族。
④A、E分别都能与D按原子个数比1∶1或2∶1形成化合物。
⑤B、C分别都能与D按原子个数比1∶1或1∶2形成化合物。
(1)写出只含有A、B、D、E四种元素的两种无水盐的化学式________________、________________。
(2)B2A2分子中存在________个σ键,________个π键。
三种短周期元素X、Y、Z,它们的原子序数之和为16,X、Y、Z三种元素的常见单质在常温下都是无色气体。已知X原子的最外层电子数是内层电子数的3倍,X和Y的单质直接化合形成气体A,X和Z的单质直接化合形成液态化合物B,Y和Z的单质直接化合形成的化合物C是一种无色有刺激性气味的气体。
请回答下列问题:
(1)Y元素在周期表中的位置是 。
(2)C可在X的单质中燃烧得到Y的单质和化合物B,利用此反应可制成新型的化学电源(KOH溶液做电解质溶液),两个电极均由多孔碳制成,通人的气体由孔隙中逸出,并在电极表面放电,则正极通入的物质是 (填物质名称);负极的电极反应式为 。
(3)C与X的单质反应生成A的化学方程式为 。
(4)常温下,C的水溶液的pH=12,则该溶液中由水电离的C(OH-)= 。若向C溶液中加入等体积、等物质的量浓度的盐酸,所得溶液中水的电离程度 (填“大于”、“等于”或“小于”)相同条件下C溶液中水的电离程度。
(5)在2L密闭容器中放入1molC气体,在一定温度进行如下反应:
2C(g)  Y2(g)+3Z2(g),反应时间(t)与容器内气体总压强(p)的数据见下表
Y2(g)+3Z2(g),反应时间(t)与容器内气体总压强(p)的数据见下表
| 时间t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| 总压强P l00 kPa | 4 | 4.6 | 5.4 | 5.8 | 6 | 6 |
该反应的化学平衡常数表达式是 (用具体物质的化学式表示);平衡时C的转化率为 。
(6)已知:①Y2(g)+2X2(g)=2YX2(g)
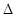 H=+67.7 kJ·mol-1。
H=+67.7 kJ·mol-1。②Y2Z4(g)+X2(g)=Y2(g)+2Z2X(g)
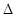 H="-534" kJ·mol-1。
H="-534" kJ·mol-1。则2Y2Z4(g)+2YX2(g)=3Y2(g)+4Z2X(g)
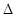 H= kJ·mol-1
H= kJ·mol-1 下表为元素周期表的一部分。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | ① | | |||||
| 二 | ② | | | ③ | ④ | ⑤ | ⑥ |
| 三 | ⑦ | ⑧ | | | | ⑨ | ⑩ |
| 四 | ? | | ? | | | | ? |
(1)表中元素________的非金属性最强;元素________的金属性最强;元素________的单质室温下呈液态(填写元素符号);
(2)表中元素⑦的原子结构示意图为_____________________;
(3)表中元素⑥⑩氢化物的稳定性顺序为________>________(填写化学式,下同);
(4)表中元素⑩和?最高价氧化物对应水化物的酸性:
________>________。
(5)表中元素②和⑦最高价氧化物对应水化物的碱性________>________。
a、b、c、d是四种短周期元素,a、b、c同周期,c、d同主族。a的原子结构示意图为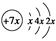 ,b与d形成的化合物的电子式为
,b与d形成的化合物的电子式为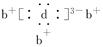 ,则下列叙述中正确的是
,则下列叙述中正确的是
( )。
| A.原子序数:a>b>c | B.d单质最活泼 |
| C.原子半径:a>c>d | D.最高价氧化物对应的水化物的酸性:d>a>c |

 Y2O3(g),其平衡常数表达式为K= 。
Y2O3(g),其平衡常数表达式为K= 。