题目内容
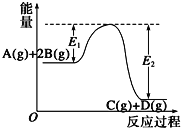
【题目】反应A(g)+B(g)C(g)+D(g)过程中的能量变化如图所示,回答下列问题. 
(1)该反应是反应(填“吸热”“放热”);
(2)当反应达到平衡时,升高温度,A的转化率(填“增大”“减小”“不变”),原因是;
(3)反应体系中加入催化剂对反应热是否有影响? , 原因是;
(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1 , E2(填“增大”“减小、”“不变”).
【答案】
(1)放热
(2)减小;该反应正反应为放热反应,升高温度使平衡向逆反应方向移动
(3)不影响;催化剂不改变平衡的移动
(4)减小;减小
【解析】解:(1)由图象可以看出反应物总能量大于生成物的总能量,则该反应的正反应为放热反应,所以答案是:放热;(2)当反应达到平衡时,该反应正反应为放热反应,升高温度使平衡向逆反应方向移动,A的转化率减小,所以答案是:减小;该反应正反应为放热反应,升高温度使平衡向逆反应方向移动;(3)催化剂能加快反应速率但不改变平衡的移动,所以反应热不变,所以答案是:不影响;催化剂不改变平衡的移动;(4)加入催化剂能降低反应物质的活化能,则E1和E2都减小,所以答案是:减小;减小.
【考点精析】根据题目的已知条件,利用吸热反应和放热反应和化学平衡状态本质及特征的相关知识可以得到问题的答案,需要掌握化学上把吸收热量的化学反应称为吸热反应;化学上把放出热量的化学反应称为放热反应;化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效).

 全优考典单元检测卷及归类总复习系列答案
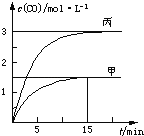
全优考典单元检测卷及归类总复习系列答案【题目】一定条件下存在反应C(s)+H2O(g)![]() CO(g)+H2(g) ΔH>0,向甲、乙、丙三个恒容容器中加入一定量C 和H2O,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法正确的是
CO(g)+H2(g) ΔH>0,向甲、乙、丙三个恒容容器中加入一定量C 和H2O,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法正确的是
容器 | 甲 | 乙 | 丙 |
容积 | 0.5 L | 0.5 L | V |
温度 | T1℃ | T2℃ | T1℃ |
起始量 | 2 mol C 1 mol H2O | 1 mol CO 1 mol H2 | 4 mol C 2 mol H2O |
A.甲容器中,反应在前15 min的平均速率v(H2)=0.1 mol·L1·min1
B.丙容器的体积V<0.5 L
C.当温度为T1℃时,反应的平衡常数K=2.25
D.乙容器中,若平衡时n(H2O)=0.4 mol,则T1<T2