题目内容
12.1个O原子中有8个电子;1个H20分子中有10个电子:1mol H20中有10mol电子;0.8mol H20中有8mol电子,这些电子的数目是8NA个(NA=6.02×1023 mol-1).分析 原子中核外电子数等于原子序数,1个O原子有8个电子;1个H20分子中有10个电子,据此计算1mol、0.8molH20中含有电子物质的量;根据N=nNA计算电子数.
解答 解:原子中核外电子数等于原子序数,1个O原子有8个电子;1个H20分子中有10个电子,1mol、0.8molH20中含有电子物质的量分别是10mol、8mol;根据N=nNA得电子数=8mol×NA/mol=8NA,
故答案为:8;10;10;8;8NA.
点评 本题考查物质的量有关计算,明确物质构成及物质的量公式中各个物理量之间关系是解本题关键,易错点是微粒中电子数计算方法.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
2.一次区分CH3COOH、CH3CH2OH、 、
、 ,四种物质的是( )
,四种物质的是( )
 、
、 ,四种物质的是( )
,四种物质的是( )| A. | 溴水 | B. | Na2CO3溶液 | C. | 水 | D. | NaHSO4溶液 |
3.有四种物质的溶液:①Ba(OH)2、②Na2SO4、③HNO3、④CuCl2,不用其他试剂就可将它们逐一鉴别出来,其鉴别顺序是( )
| A. | ④①②③ | B. | ①③④② | C. | ④③②① | D. | ①④②③ |
20.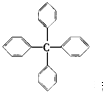 甲烷分子中的4个氢原子都可以被取代,若甲烷分子中的4个氢原子都被苯基取代,可以得到的分子如图,对该分子的描述,不正确的是( )
甲烷分子中的4个氢原子都可以被取代,若甲烷分子中的4个氢原子都被苯基取代,可以得到的分子如图,对该分子的描述,不正确的是( )
 甲烷分子中的4个氢原子都可以被取代,若甲烷分子中的4个氢原子都被苯基取代,可以得到的分子如图,对该分子的描述,不正确的是( )
甲烷分子中的4个氢原子都可以被取代,若甲烷分子中的4个氢原子都被苯基取代,可以得到的分子如图,对该分子的描述,不正确的是( )| A. | 分子式为C25H20 | |
| B. | 所有的碳原子不可能都在同一平面上 | |
| C. | 所有原子一定在同一平面上 | |
| D. | 此物质属于芳香烃类物质 |
7.在一定条件下,NO跟NH3可以发生反应:6NO+4NH3=5N2+6H2O,关于该反应下列说法中不正确的是( )
| A. | H2O既不是氧化产物也不是还原产物 | |
| B. | 该反应中被氧化和被还原的氮元素的质量比是3:2 | |
| C. | 若有2mol NH3完全反应,共转移12mol电子 | |
| D. | NO是氧化剂,NH3是还原剂 |
4.下列各组物质在通常条件下既可由置换反应得到,又可由复分解反应制得的是( )
| A. | Na2O | B. | NaOH | C. | NaHCO3 | D. | Na2O2 |
13.用NA表示阿伏加德罗常数的值,下列叙述不正确的是( )
| A. | 标准状况下,22.4L Cl2溶于水,转移的电子数目小于 NA | |
| B. | 常温常压下,18 g H2O中含有的原子总数为3 NA | |
| C. | 0.1 moI•L-1的CH3COOH溶液中所含的离子和分子总数为0.1NA | |
| D. | 乙烯和聚乙烯组成的14 g混合物中原子总数为3 NA |
14.下列有关实验操作、现象与结论对应关系正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向盛有Fe(NO3)2溶液的试管中加入0.1mol•L-1硫酸溶液 | 试管口出现红棕色气体 | 溶液中NO3-被Fe2+还原为NO2 |
| B | H2S通入CuSO4溶液中 | 溶液中出现黑色沉淀 | 酸性:H2S>H2SO4溶液 |
| C | 在CuSO4溶液中加入KI溶液,再加入苯,振荡、静置 | 有白色沉淀生成,苯层呈紫红色 | 白色沉淀可能为CuI |
| D | 将一小块钠投入到CuSO4溶液中 | 有无色无味的气体放出,且出现蓝色沉淀 | 氧化性:H+>Cu2+ |
| A. | A | B. | B | C. | C | D. | D |