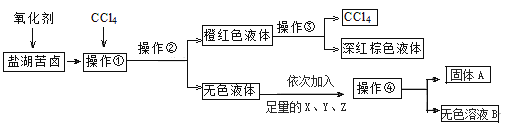
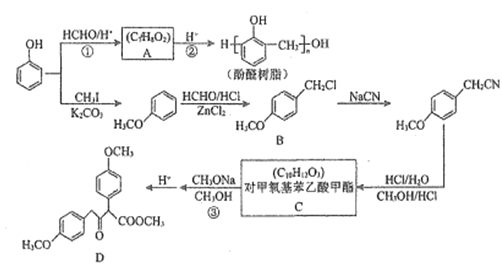
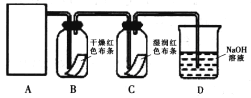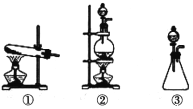��Ŀ����
����Ŀ���������NOx���Ǵ�����Ⱦ��֮һ����ҵ����һ�����¶Ⱥʹ��������£�����NH3������NOx����Ⱦ���������ֶԻ����������ʡ�
��1����д��NH3��NO2��Ӧ�Ļ�ѧ����ʽ____��
��2����д��ʵ�������ɹ���������ȡ�����Ļ�ѧ����ʽ__��
�����ռ�һƿ����İ�����ѡ����ͼ�е�װ�ã�������˳��Ϊ������װ����____��������������Сд��ĸ��ʾ��
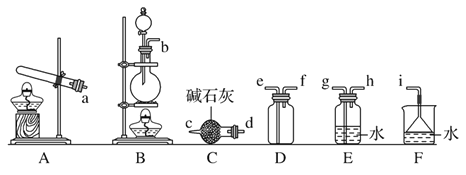
��3����ⷨ��������������������ɻ������ᣬ���нϸߵĻ���Ч��;���Ч�档ʵ����ģ���ⷨ����NOx��װ����ͼ��ʾ��ͼ�е缫��Ϊʯī�缫��������NO2�������ģ���ⷨ����ʵ�顣

��д�����ʱNO2������Ӧ�ĵ缫��Ӧʽ��___��
�����б�״����2.24LNO2�����գ�ͨ�������ӽ���Ĥ��ֻ����������ͨ������H+Ϊ__mol��
���𰸡�6NO2��8NH3![]() 7N2��12H2O 2NH4Cl+Ca(OH)2
7N2��12H2O 2NH4Cl+Ca(OH)2![]() CaCl2+2NH3��+2H2O d��c��f��e��(dc)��i NO2��e-��H2O��NO3-��2H+ 0.1
CaCl2+2NH3��+2H2O d��c��f��e��(dc)��i NO2��e-��H2O��NO3-��2H+ 0.1
��������
��1������֪һ�����¶Ⱥʹ��������£�����NH3������NOx����Ⱦ���������ֶԻ����������ʣ��䷴Ӧ�Ļ�ѧ����ʽΪ6NO2��8NH3![]() 7N2��12H2O���𰸣�6NO2��8NH3
7N2��12H2O���𰸣�6NO2��8NH3![]() 7N2��12H2O��
7N2��12H2O��
��2����д��ʵ�������ɹ���������ȡ������ԭ��ΪCa(OH)2��NH4Cl,�ڼ��ȵ������·�����Ӧ�����ɰ������Ȼ��ƺ�ˮ���䷴Ӧ�Ļ�ѧ����ʽΪ��2NH4Cl+Ca(OH)2![]() CaCl2+2NH3��+2H2O���𰸣�2NH4Cl+Ca(OH)2
CaCl2+2NH3��+2H2O���𰸣�2NH4Cl+Ca(OH)2![]() CaCl2+2NH3��+2H2O��
CaCl2+2NH3��+2H2O��
��AΪ����װ�ã��Ƶõİ���Я��ˮ������ͨ����ʯ�ҽ��и����������Ϊ��a��d��c,��װ��D�ռ������������ܶȱȿ���С������f������e�����������ӣ�Ϊ�˴�������İ�������Ҫ��Fװ�ý��д�����������������ˮ������Ҫ���÷�����װ�ã�����װ��E �е�I,��˳��Ϊ������װ�á�d��c��f��e��i �����Ա���𰸣�d��c��f��e��i��
��3������ͼ��֪���ʱNO2������Ӧ�ɻ���HNO3���ݵ���غ��ԭ�Ӹ����غ㣬��Ͻ��ʻ����ɵõ缫��ӦʽNO2+H2O-e-=2H++ NO3-���𰸣�NO2+H2O-e-=2H++ NO3-;
�ڱ�״����2.24 L NO2��0.1 mol�μӷ�Ӧ��ת�Ƶ�����Ϊ0.1 mol����������H2����H+Ϊ0.1 mol����ͨ�������ӽ���Ĥ(ֻ����������ͨ��)��H+Ϊ0.1 mol���𰸣�0.1mol��

����Ŀ���о�ú�ĺ������ü�CO2���ۺ�Ӧ��������Ҫ�����塣��ش���������:
I.ú������
��֪ú�����������漰�Ļ�����ѧ��Ӧ�У�
C��s��+H20��g��![]() CO��g��+H2��g�� ��H=+131kJ/mol
CO��g��+H2��g�� ��H=+131kJ/mol
��CO��g��+3H2��g��![]() CH4��g��+H2O��g�� ��H=akJ/mol
CH4��g��+H2O��g�� ��H=akJ/mol
�������Ϸ�Ӧ������ػ�ѧ�������������±���
��ѧ�� |
| H-H | H��C | H-O |
E/��kJ/mol�� | 1072 | 436 | 414 | 465 |
��1��úֱ�Ӽ��黯��ӦC��s��+2H2��g��![]() CH4��g���ġ�HΪ_______kJ/mol���÷�Ӧ��______����{�¡����¡������Է����С�
CH4��g���ġ�HΪ_______kJ/mol���÷�Ӧ��______����{�¡����¡������Է����С�
��.�ϳɵ�̼ϩ��
�����Ϊ1 L���ܱ������У�����1molCO2��2.5molH2��������Ӧ��
2C02��g��+6H2��g��![]() C2H4��g��+4H20��g�� ��H=-128kJ/mol������¶ȶԴ�����Ч�ʺ� C02ƽ��ת���ʵ�Ӱ����ͼ��ʾ��
C2H4��g��+4H20��g�� ��H=-128kJ/mol������¶ȶԴ�����Ч�ʺ� C02ƽ��ת���ʵ�Ӱ����ͼ��ʾ��
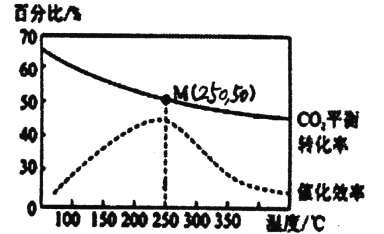
��2��ͼ�е���ʱ�������¶����ߴ����Ĵ�Ч����ߣ���C02��ƽ��ת����ȴ�������ͣ���ԭ����__________��
��3��250��ʱ���÷�Ӧ��ƽ�ⳣ��KֵΪ__________��
��.�ϳɼ״�
�ں���2 L�ݻ�������ܱ������У�����lmolC02��3molH2��������Ӧ��C02��g��+3H2��g��![]() CH30H��g��+H20��g������ò�ͬʱ�̷�Ӧǰ��������ѹǿ�仯��p��/pǰ�����±���
CH30H��g��+H20��g������ò�ͬʱ�̷�Ӧǰ��������ѹǿ�仯��p��/pǰ�����±���
ʱ��/h | 1 | 2 | 3 | 4 | 5 | 6 |
p��/pǰ | 0.90 | 0.85 | 0.82 | 0.81 | 0.80 | 0.80 |
��4����Ӧǰ1Сʱ�ڵ�ƽ����Ӧ����V��H2��Ϊ_________mol/��L��h�������¶���C02��ƽ��ת����Ϊ_________��
IV.�����ת�����Ҵ�
��5��������Աͨ������ʵ�鷢�֣�C02����������ˮ��Һ�е�������Ҵ����������Ҵ��ķ�Ӧ������_________���������������������õ缫�ķ�ӦʽΪ_________��