题目内容
【题目】(1)下列各组物质属于同素异形体________;属于同位素是________;属于同一种物质是________;属于同系物是________。(写序号)
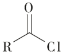
①红磷与白磷;②12C与14C;③S2与S8;④235U与238U;⑤干冰与二氧化碳;⑥CH4与CH3CH3;⑦ ![]() 与
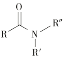
与 ![]() ;⑧CH3CH=CH2和CH2=CH2。
;⑧CH3CH=CH2和CH2=CH2。
(2)已知A的产量可以用来衡量一个国家的石油化工发展水平,请写出工业上用A制备酒精的化学方程式________。
(3)在一定体积的 18 mol/L的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为 0.9 mol。则浓硫酸的实际体积________ (填“大于”“小于”或“等于”)100 mL。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如 KNO3溶液),则该反应的离子方程式_________。
【答案】①③ ②④ ⑤⑦ ⑥⑧ CH2=CH2+H-OH![]() CH3-CH2-OH 大于 3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
CH3-CH2-OH 大于 3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
【解析】
(1)根据有关概念分析、判断;
(2)A的产量可以用来衡量一个国家的石油化工发展水平,则A是乙烯,乙烯与水在一定条件下发生加成反应制取酒精;
(3)Cu与浓硫酸反应产生CuSO4、SO2、H2O,与稀硫酸不能反应,在酸性条件下Cu、H+、NO3-会发生氧化还原反应,据此分析解答。
(1)同素异形体是同一元素组成的不同性质的单质;同位素是质子数相同而中子数不同的原子;同一物质分子式相同,化学性质相同,物理性质可能不同;同系物是结构相似,在分子组成上形成1个或若干CH2原子团的物质;
①红磷与白磷是磷元素的两种不同性质的单质,二者互为同素异形体;
②12C与14C是C元素的两种不同的原子,二者互为同位素;
③S2与S8是硫元素的不同性质的单质,二者互为同素异形体;
④235U与238U的质子数相同,中子数不同,二者互为同位素;
⑤干冰是固体CO2,因此干冰与二氧化碳是同一物质;
⑥CH4与CH3CH3都属于烷烃,结构相似,在分子组成上形成1个CH2原子团,互为同系物;
⑦给出的物质结构可看作是甲烷分子中2个H原子被Cl原子取代产生的物质,由于甲烷是正四面体结构,分子中任何两个化学键都相邻,所以![]() 与
与 ![]() 表示的是同一物质;
表示的是同一物质;
⑧CH3CH=CH2和CH2=CH2都属于烯烃,结构相似,在分子组成上形成1个CH2原子团,二者互为同系物;
综上所述可知:属于同素异形体的是①③;属于同位素的是②④;属于同一种物质的是⑤⑦;属于同系物的是⑥⑧;
(2)已知A的产量可以用来衡量一个国家的石油化工发展水平,则A是乙烯,结构简式是CH2=CH2,乙烯分子中含有不饱和的碳碳双键,与水在一定条件下发生加成反应制取乙醇(俗称酒精),该反应的化学方程式为:CH2=CH2+H-OH![]() CH3-CH2-OH;
CH3-CH2-OH;
(3)Cu与浓硫酸在加热时反应产生CuSO4、SO2、H2O,反应方程式为:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O。在该反应中,每有2 mol H2SO4发生反应,其中就有1 mol被还原产生SO2,若被还原的硫酸为0.9 mol,则反应消耗硫酸的物质的量为n(H2SO4)=2×0.9 mol=1.8 mol,已知浓硫酸物质的量浓度为18 mol/L,则理论上需要浓硫酸体积V=
CuSO4+SO2↑+2H2O。在该反应中,每有2 mol H2SO4发生反应,其中就有1 mol被还原产生SO2,若被还原的硫酸为0.9 mol,则反应消耗硫酸的物质的量为n(H2SO4)=2×0.9 mol=1.8 mol,已知浓硫酸物质的量浓度为18 mol/L,则理论上需要浓硫酸体积V=![]() =0.1 L=100 mL,但由于只有浓硫酸在加热时能够与Cu反应,随着反应的进行,硫酸溶液浓度变稀,反应就不再发生,因此实际消耗浓硫酸的体积大于100 mL。在反应后的溶液中含有未反应的H2SO4,使溶液显酸性,在酸性条件下Cu、H+、NO3-会发生氧化还原反应,产生Cu2+、NO、H2O,反应的离子方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O。
=0.1 L=100 mL,但由于只有浓硫酸在加热时能够与Cu反应,随着反应的进行,硫酸溶液浓度变稀,反应就不再发生,因此实际消耗浓硫酸的体积大于100 mL。在反应后的溶液中含有未反应的H2SO4,使溶液显酸性,在酸性条件下Cu、H+、NO3-会发生氧化还原反应,产生Cu2+、NO、H2O,反应的离子方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O。

 金钥匙试卷系列答案
金钥匙试卷系列答案